Comparaison des modèles de diffusion dans les tumeurs de Wilms et le tissu rénal controlatéral normal
Mar 07, 2022
Contact:tina.xiang@wecistanche.com
Résumé
ObjectifL'ADC (coefficient de diffusion apparent) dérivé de l'imagerie pondérée en diffusion (DWI) s'est révélé prometteur en tant que biomarqueur d'imagerie quantitative non invasif dansTumeurs de Wilms. Cependant, de nombreux modèles non gaussiens pourraient être appliqués à DWI. Cette étude visait à comparer la pertinence de quatrela diffusionmodèles (monoexponentiel, IVIM [Intravoxel Incoherent Motion], exponentiel étiré et kurtosis) dans les tumeurs de Wilms et le controlatéral non affectéreins.
Matériels et méthodes Les données DWI ont été examinées rétrospectivement (110 ensembles de données sur les tumeurs de Wilms et 75 sur les reins normaux). La qualité de l'ajustement pour chaque modèle a été mesurée par voxel à l'aide des critères d'information d'Akaike (AIC). L'AIC moyen a été calculé pour chaque volume tumoral (ou tissu rénal normal controlatéral). Les ANOVA unidirectionnelles avec correction de Greenhouse-Geisser et les tests post hoc utilisant la correction de Bonferroni ont évalué les différences significatives entre les valeurs AIC ; l'AIC le plus bas indiquant le modèle optimal.
RésultatsL'IVIM et l'exponentielle étirée ont fourni les meilleurs ajustements aux données DWI de la tumeur de Wilms. IVIM a fourni le meilleur ajustement pour les données sur les reins normaux. Mono exponentielle était la méthode d'ajustement la moins appropriée pour les données sur la tumeur de Wilms et sur les reins normaux.
DiscussionLe signal pondéré en diffusion dansTumeurs de Wilmset normaletissu rénalne présente pas de décroissance mono-exponentielle et est mieux décrite par des modèles de diffusion non gaussiens.
Mots cléstumeur de Wilms. Reins. La diffusion

Pour plus d'informations, cliquez ici
Introduction
La tumeur de Wilms est la tumeur rénale pédiatrique la plus fréquente [1], et en Europe, les patients sont traités par chimiothérapie avant la chirurgie pour réduire la taille de la tumeur [2]. Après une néphrectomie complète ou partielle, l'analyse histologique classe la tumeur en sous-type selon le type cellulaire prédominant [3]. Les patients subiront souvent plusieurs IRM pour surveiller la réponse au traitement, l'imagerie pondérée en diffusion (DWI) étant fréquemment acquise.
Le coefficient de diffusion apparent (ADC) peut être dérivé de DWI en appliquant un ajustement mono-exponentiel (Eq.1) aux données de diffusion.
(1)S(b)= Se-b.ADC
où S(b) est le signal à une valeur b donnée, et S. est le signal sans pondération de diffusion.
L'ADC s'est révélé très prometteur en tant qu'outil d'imagerie quantitative dans la tumeur de Wilms. Par exemple, l'ADC a été utilisé pour distinguer les tumeurs bénignes des tumeurs malignes (un sous-ensemble de ce
cohorte étant les tumeurs de Wilms) [4], séparer le neuroblastome de la tumeur de Wilms [5], surveiller la réponse à la chimiothérapie [6, 7], identifier les sous-types histologiques [7] et aider à identifier le tissu nécrotique de la tumeur de Wilms [8].
Bien que l'ADC soit un paramètre utile, il existe d'autres modèles non gaussiens (VIM [9] [ntravoxel Incoherent Motion], exponentiel étiré [10] et kurtosis [11]) qui peuvent être appliqués aux données DWI pour produire une large gamme de mesures de diffusion. IVIM (Eq.2) est un modèle bi-exponentiel qui décrit non seulement le mouvement de l'eau dans l'espace extra-vasculaire, mais également dans le réseau micro capillaire orienté de manière aléatoire. Il produit les paramètres D(le coefficient de diffusion libre de l'influence de l'eau à écoulement rapide dans le réseau capillaire, appelé diffusion lente), D*(le coefficient de diffusion dû au mouvement aléatoire de l'eau dans le sang dans le réseau capillaire-diffusion rapide), et f(la fraction volumique associée à la composante à écoulement rapide). (2)S(b)= Donc[(1-f)e(-bD plus fel-b(D plus D')
Le modèle exponentiel étiré (Eq. 3) décrit l'hétérogénéité de la diffusion dans un seul voxel, décrivant l'écart par rapport à une décroissance mono-exponentielle. Il produit les paramètres DDC (le coefficient de diffusion distribué) et a (le paramètre d'étirement pour décrire l'écart par rapport à la diffusion homogène).
(3)S(b)= S,e(-(b.DDC)")
Le modèle d'aplatissement (Eq.4) décrit l'écart par rapport au déplacement des molécules d'eau suivant une distribution gaussienne et produit les paramètres D (le coefficient de diffusion corrigé du déplacement non gaussien) et K (l'aplatissement).
(4)S(b)= Soe-bD plus b2D, ?K/6
Ces modèles ont le potentiel de fournir des informations supplémentaires concernant la microstructure des tissus. De plus, il a été démontré qu'ils fournissent des descriptions supérieures des données de diffusion par rapport au modèle mono-exponentiel dans le cancer du rectum [12], les métastases osseuses du cancer de la prostate [13], le cancer de l'ovaire [14] et le tissu rénal sain [15]. Cependant, il existe peu de recherches sur l'application de ces modèles dans la tumeur de Wilms où ils peuvent être utiles, en raison de l'environnement cellulaire très hétérogène du tissu tumoral. De plus, on suppose qu'en raison des niveaux élevés de perfusion dans lereins, et que IVIM est conçu pour tenir compte d'une composante liée à la perfusion dans le signal de diffusion, ce modèle peut fournir un ajustement supérieur à ces données DWI [16].
Le but de cette recherche était de déterminer si ces modèles (VIM, exponentiel étiré et kurtosis) fournissent des ajustements supérieurs au signal pondéré en diffusion par rapport à un modèle mono-exponentiel, dans les tumeurs de Wilms et la normale controlatéraleun rein. La qualité de l'ajustement a été calculée à l'aide du critère d'information d'Akaike (AIC) [17], qui pénalise les modèles contenant plus de paramètres libres que ceux pris en charge par les données brutes. De plus, comme objectif secondaire, les tumeurs de Wilms ont été séparées par sous-type histologique pour déterminer si certains modèles favorisaient certains sous-types.

Matériels et méthodes Population étudiée
L'approbation éthique institutionnelle a été accordée et a renoncé à la nécessité d'un consentement pour cette étude monocentrique. Un examen rétrospectif de 10- ans (avril 2007- mars 2017) du système d'imagerie radiologique de notre établissement a été réalisé pour toutes les données d'IRM abdominales chez les enfants présentant un diagnostic histologique prouvé detumeur de Wilms. Les critères d'inclusion étaient ceux avec plusieurs données de valeur b DWI (y compris une valeur b maximale de 1000 s/mm2) et la taille de la tumeur couvrant au moins 2 tranches axiales sur DWI. DWI avec des artefacts de mouvement extrême ont également été supprimés. Les données IRM ont été recueillies auprès de patients atteints de la tumeur de Wilms avant et après la chimiothérapie. Les sous-types histologiques ont été confirmés après la chirurgie pour un sous-ensemble de tumeurs. Pour les données rénales normales, le rein non affecté controlatéral a été utilisé, sauf chez les patients atteints d'une maladie bilatérale.
IRM
Toutes les images ont été réalisées sur un scanner Siemens Magnetom Avanto de 1,5 T équipé de gradients de 40 mT/m. Selon la taille du patient, une ou deux bobines de matrice corporelle ont été utilisées pour obtenir une couverture complète (conception à 6 éléments, Siemens). Les patients étaient soit éveillés, soit anesthésiés selon leur âge.
La valeur b multiple DWI a été obtenue pour tous les patients et a été acquise pendant la respiration libre. Le protocole DWI était le suivant :7 ou 8b valeurs dans 3 directions orthogonales(0, 50,100,250,500,750,1000 s/mm²ou 0,50,100,150,200,250,500,1000 s/mm²)épaisseur de tranche∶6 mm, TR/TE : 2 800 ms/89 ms, le champ de vision : 350 × 350 mm, la taille du voxel : 1,4 × 1,4 × 6 mm, le nombre de tranches : 19, la taille de la matrice : 128 × 96 × 19. Neuf moyennes ont été acquises pour chaque valeur et des images de trace (moyenne sur 3 directions) ont été utilisées pour l'analyse Des séquences cliniques standard ont également été acquises en conjonction, y compris T w avec suppression de la graisse avant et après l'administration d'un produit de contraste à base de gadolinium ; tous les détails des séquences d'imagerie clinique peuvent se trouve dans [18].
Post-traitement
La diffusionles données ont été traitées à l'aide des images de trace et des routines d'ajustement de modèles internes conçues dans Matlab (version 2019a, MathWorks Inc., Natick, MA, États-Unis) sur une base voxel par voxel en utilisant quatre modèles de diffusion différents : monoexponentiel (Eq. 1), IVIM (Eq.2), exponentiel étiré (Eq.3) et aplatissement (Eq.4).
Dans chaque cas, Swas défini comme le signal à b{{{{10}}}}, et pour le modèle mono-exponentiel, un ajustement linéaire de In(S/S.) contre toutes les valeurs b était effectué. Pour les modèles non gaussiens, l'ajustement a été effectué à l'aide de l'algorithme non linéaire des moindres carrés de Levenberg-Mar-quart (en utilisant la fonction 'lsq-curve-fit dans Matlab), sur toutes les valeurs b (à l'exception du modèle IVIM). Pour le modèle IVIM, premièrement, un ajustement linéaire de In(S/S.) contre b a été calculé à des valeurs b élevées (200-1000 s/mm2) pour déterminer la valeur de D. Suite à cela, D* et f étaient ajustés simultanément (avec un D fixe). D n'avait aucune contrainte sur les limites supérieures et f était contraint entre 0 et 1. Pour le modèle exponentiel étiré, DDC n'avait pas de conditions de limite supérieure et était contraint entre 0 et 1. Pour l'aplatissement, ni Dk ni K n'étaient limités par des limites supérieures, et K avait une limite inférieure de 0.
Régions d'intérêt (ROI)
Les retours sur investissement ont été générés à l'aide du logiciel Mango (Research Imaging Institute, UTHSCSA). années consacrées à la radiologie pédiatrique). Le tissu rénal normal a également été défini sur les images b0 en utilisant le rein controlatéral (à l'exclusion de ceux atteints d'une maladie bilatérale) autour de tout le volume rénal et les zones à haut débit, telles que les zones qui entourent le bassinet rénal, ont été exclues ; un exemple peut être vu dans la figure 1. Toutes les analyses concernant les comparaisons de modèles se sont limitées à ces retours sur investissement.
Analyse de comparaison de modèles
L'AIC a été utilisé pour comparer les quatre modèles (monoexponentiel, IVIM, exponentiel étiré et aplatissement). Pour chaque voxel dans les ROI tumorales et les ROI rénales normales. L'AIC a été calculé par modèle. L'AIC moyen a été calculé sur l'ensemble du volume de retour sur investissement par modèle. Les valeurs moyennes de l'AIC pour chaque modèle ont ensuite été comparées à l'aide d'une ANOVA à mesures répétées unidirectionnelle avec une correction de Greenhouse-Geis-ser pour tenir compte de la variance non égale, et des tests post hoc ont été effectués à l'aide de la correction de Bonferroni. Une différence significative a été définie comme p<0.05.anovas were="" calculated="" for="" the="" entire="" wilms'tumour="" and="" normal="" kidney="" populations,="" as="" well="" as="" within="" different="" subgroups="" (pre-chemotherapy,="" post-chemotherapy,="" and="" different="" b="" value="" acquisitions="" [7="" and="" 8="" b="" value="" ranges]).="" additionally,="" models="" were="" compared="" between="" wilms'tumour="" histological="" subtypes="" to="" determine="" whether="" a="" certain="" subtype="" favoured="" a="" particular="" model.="" the="" post-chemotherapy="" data="" were="" used="" for="" this="" comparison="" as="" it="" was="" the="" nearest="" time="" point="" to="">
Résultats
Population étudiée
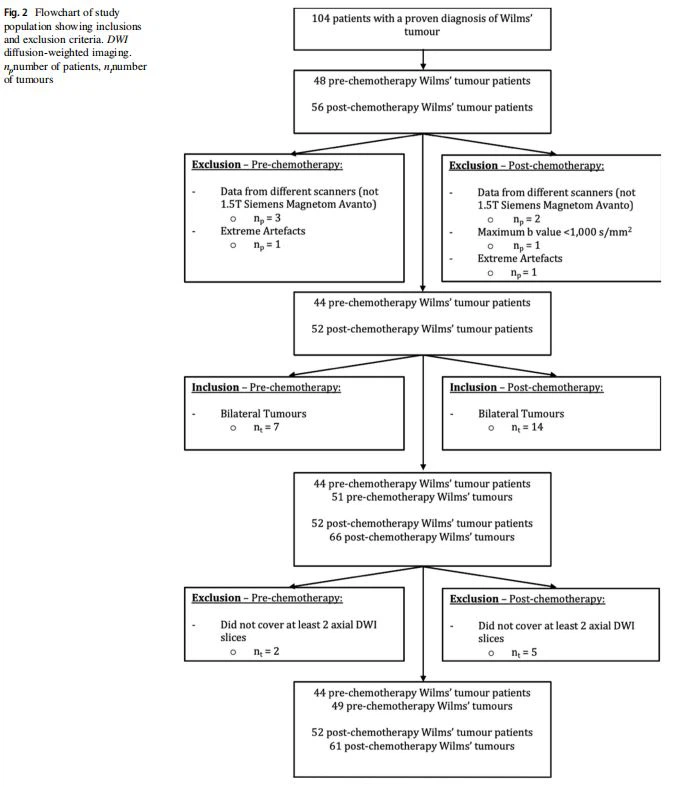
Un total de 11 0 tumeurs de Wilms ont été incluses pour l'analyse comparative des modèles de diffusion ; consistant en 49 tumeurs pré-chimiothérapie et 61 tumeurs post-chimiothérapie (38 des tumeurs pré-chimiothérapie ont été incluses dans les 61 cohortes post-chimiothérapie). Un organigramme détaillant les inclusions et les exclusions de cas peut être vu dans la Fig.2. L'âge moyen des patients lors de leur scanner pré-chimiothérapie était de 2,43 ans (SD : 2,2) et l'âge moyen lors de leur scanner post-chimiothérapie était de 3,0 ans (SD : 2,8).
The diffusion data were acquired using either 7 or 8 b values(0,50,100,250,500,750,1000 s/mm²or 0,50,100,150,200,250,500,1000 s/mm>). Cela était dû au changement de protocole au cours de la période de cette étude, pour des raisons non liées à cette étude. Quarante-neuf tumeurs avaient le protocole de valeur 7b (22 pré-chimiothérapie et 27 post-chimiothérapie), et 61 tumeurs avaient le protocole de valeur 8b (27 pré-chimiothérapie et 34 post-chimiothérapie).
Sur les 61 tumeurs post-chimiothérapie, 56 avaient des sous-types histologiquement confirmés : 7 blastémiques, 9 épithéliaux, 13 stromaux, 8 régressifs, 18 mixtes et 1 complètement nécrotique. Les sous-types ont été définis selon le protocole SIOP-2001 [3].
Le rein non affecté controlatéral a été utilisé comme données sur le rein normal. En raison de la nécessité d'exclure les cas bilatéraux, un total de 75 ensembles de données sur les reins normaux ont été inclus ;38de patients qui avaient reçu une chimiothérapie et 37 de patients qui n'en avaient pas reçu. Sur les 75 ensembles de données sur les reins normaux, 31 avaient le protocole de valeur 7b (15 avant la chimiothérapie et 16 après la chimiothérapie) et 44 avaient le protocole de valeur 8b (22 avant et 22 après la chimiothérapie).

Résultats de la tumeur de Wilms
Les ANOVA unidirectionnelles avec une correction de Greenhouse-Geisser ont révélé que les valeurs de l'AIC différaient significativement entre les modèles de diffusion, dans toutes les conditions :cohorte entière :(F(1,08, 117,91)=157.08,p=1.68 ×10-24), pré-chimiothérapie :(F(1.05,50.53)=79.35,p=3.11×10-12),post-chimiothérapie :( F(1.13,67.92)=85.92,p=1.34×10-14),7b valeurs :(F(1.21,58.16)=76.23,p{ {39}}.10×10-13),et8b valeurs :(F(1.04,62.49)=95.51,p=1.68×10-14).
La figure 3 montre les boîtes à moustaches de chaque condition, avec des barres significatives mettant en évidence les résultats des tests post hoc à l'aide de la correction de Bonferroni. Dans toutes les conditions, les valeurs d'AIC pour le modèle mono-exponentiel étaient significativement plus élevées que les trois autres modèles, ce qui indique qu'il s'agissait du modèle le moins approprié pour les données sur la tumeur de Wilms. Pour l'ensemble des cohortes tumorales et post-chimiothérapie de Wilms, l'exponentielle étirée était le meilleur modèle pour ajuster les données de diffusion, car cela fournissait les valeurs AIC les plus basses. La figure 4 montre un exemple de la façon dont les modèles s'adaptent au signal de désintégration par diffusion dans un seul voxel d'une tumeur de Wilms post-chimiothérapie.
Pour la cohorte pré-chimiothérapie et lorsque les données ont été divisées en plages de valeurs de 7 et 8 b, les modèles IVIM et exponentiel étendu ont été jugés les plus appropriés, sans différence significative entre les valeurs AIC pour ces deux modèles.
Additionally, one-way ANOVAs were used to investigate whether the best fit model was related to Wilms'tumour histological subtypes, using the post-chemotherapy data as they were the closest timepoints to histology. Only one tumour was classified as necrotic and was therefore removed from this section of the analysis. Figure 5 shows the AIC values for each subtype based on different diffusion models. There were no significant differences between AIC values across the subtypes (blastemal [n=7], epithelial [n=9], mixed [n=18], stromal [n=13], regressive [n=8]), for any of the models (p>0.05).
Résultats rénaux normaux
Les ANOVA unidirectionnelles avec une correction de Greenhouse-Geisser ont également révélé que les valeurs d'AIC différaient significativement entre les modèles de diffusion, dans toutes les conditions pour les données rénales normales : cohorte entière : (F(1,51,85,2)=276. 07, p=2.57×10-30), pré-chimiothérapie :(F(1.43, 41.13)=119.38,p=1.16×{{22} }), post-chimiothérapie : (F(1.16,42.81)=157.33,p=1.10×10-15,7 valeurs b :(F(1.14,34.10){{ 38}}.49,p=1.06×10-1),et 8b valeurs :(F(1.14,49.10)=193.30,p=1.19× 10-19.
La figure 6 montre les boîtes à moustaches de chaque condition, avec des barres de signification mettant en évidence les résultats des tests post hoc à l'aide de la correction de Bonferroni. Les données sur les reins normaux ont fourni des résultats similaires aux données sur la tumeur de Wilms : dans toutes les conditions, les valeurs d'AIC pour le modèle mono-exponentiel étaient significativement plus élevées que les trois autres modèles, ce qui indique qu'il s'agissait du modèle le moins approprié pour les données sur les reins normaux. Contrairement aux données sur la tumeur de Wilms, pour toutes les conditions, les données sur les reins normaux ont montré que l'IVIM fournissait les valeurs AIC les plus basses, indiquant qu'il s'agissait du modèle le plus approprié pour ces données de diffusion. La figure 7 montre un exemple de la façon dont les modèles s'adaptent au signal de décroissance de diffusion dans les données de rein normal controlatéral d'un patient post-chimiothérapie présentant une tumeur de Wilms.

Discussion
Cette étude a comparé quatre modèles dela diffusion(monoexponentiel, IVIM, exponentiel étiré et kurtosis) en fonction de leur adaptation à la décroissance du signal DWI, selon l'AIC. Ces comparaisons ont été faites dans les tumeurs de Wilms, à la fois avant et après la chimiothérapie, et sur le rein non affecté controlatéral, comme mesure du tissu rénal normal. Les données de diffusion provenaient des plages de valeurs 7 et 8 b. Pour les données sur la tumeur de Wilms, il a été démontré que le modèle exponentiel étiré fournissait le meilleur ajustement global. Ce résultat a été maintenu lorsque l'analyse a été confinée au groupe post-chimiothérapie. Cependant, lorsque l'analyse était axée sur les données pré-chimiothérapie et lorsqu'elles étaient séparées par l'acquisition de la valeur b, il n'y avait pas de différences significatives entre l'IVIM et l'exponentiel étiré, les deux modèles fournissant les valeurs AIC les plus basses. De plus, il n'y avait pas de préférences de modèle particulières lorsque les tumeurs étaient regroupées par sous-type histologique. Pour les données sur les reins normaux, IVIM a fourni le meilleur ajustement dans toutes les analyses. Le modèle mono-exponentiel s'est avéré être le modèle le moins approprié selon l'AIC ; fournissant des valeurs AIC significativement plus élevées par rapport aux autres modèles pour les deuxtumeur de Wilmset ensembles de données sur les reins normaux.
La principale conclusion de cette enquête était que les modèles non gaussiens fournissaient de meilleures descriptions des données de diffusion par rapport aux modèles monoexponentiels, à la fois dans la tumeur de Wilms et dans le tissu rénal normal. L'écart par rapport à une décroissance mono-exponentielle a déjà été mis en évidence et exploré : il a été montré qu'il y avait une baisse rapide du signal à des valeurs plus basses suivie d'une baisse plus progressive à des valeurs de b plus élevées dans le foie [19]. Il a été suggéré que ce déclin initial était dû à la perfusion vasculaire, car des valeurs b inférieures seraient sensibles à l'atténuation du signal de la perfusion [9], ce qui rend le modèle IVIM bien adapté à ces données. Cela s'est avéré être le cas dans le tissu rénal sain [20,21], où le signal s'est avéré être bi-exponentiel par opposition à monoexponentiel ; car le rein est un organe bien perfusé. La présente étude appuie ces résultats car l'IVIM a été préféré aux autres modèles dans le tissu rénal normal. Cette constatation a été maintenue dans l'ensemble de données sur les reins normaux post-chimiothérapie, ce qui suggère que le traitement n'a pas affecté le tissu rénal normal d'une manière qui pourrait être détectée par les données DWI.


Le modèle exponentiel étiré a fourni un bon ajustement aux données tumorales de DWI Wilms. Les études mentionnées précédemment sur le cancer rectal et le tissu rectal sain [12], les métastases osseuses du cancer de la prostate [13] et le cancer de l'ovaire [14], ont toutes montré que ce modèle offre le meilleur ajustement aux données DWI par rapport à IVIM et monoexponentiel. Le modèle exponentiel étiré fournit deux paramètres, et DDC ; bien que la base physiologique exacte de soit inconnue, on pense qu'elle représente l'hétérogénéité tissulaire, une valeur inférieure suggérant un environnement plus hétérogène [10]. Le tissu tumoral de Wilms étant très hétérogène, il n'est pas surprenant que le modèle exponentiel étiré décrive bien ces données.
En plus du modèle exponentiel étiré, l'IVIM a fourni un ajustement tout aussi bon aux tumeurs de Wilms avant la chimiothérapie, alors que ce n'était pas le cas après le traitement. Après le traitement, il est probable qu'il y ait une augmentation du tissu nécrotique et donc une diminution de la perfusion, par conséquent IVIM (un modèle qui se concentre sur les effets de la perfusion) peut devenir moins approprié.
Aucun sous-type histologique particulier n'a semblé favoriser un certain modèle, cependant, les nombres dans chaque groupe étaient petits. De plus, il est important de noter que les sous-types histologiques sont définis après analyse d'une seule sous-section
de tout le volume tumoral. Les tumeurs de Wilms sont très hétérogènes et à travers une même tumeur, il y aura des zones d'environnements cellulaires distincts. Les voxels au sein de ces régions distinctes peuvent avoir montré des préférences de modèle de diffusion variables. Cependant, en raison du manque d'histologie avancée, cette analyse n'a pas été possible.

L'utilisation de modèles non gaussiens peut non seulement fournir de meilleurs ajustements aux données, mais peut également fournir des informations cliniques supplémentaires. Par exemple, il a été démontré que le D, issu de l'aplatissement, pourrait fournir une plus grande précision diagnostique par rapport à l'ADC pour différencier la tumeur de la non-tumorale dans le cancer du pancréas [22]. De plus, (exponentiel étiré) avait des niveaux de sensibilité et de spécificité plus élevés lors de la discrimination entre un angiomyolipome graisseux minimal et un carcinome à cellules rénales par rapport à l'ADC [23]. De plus, D et f(IVIM) se sont révélés prometteurs pour mettre en évidence la fonction rénale, les deux paramètres étant liés au taux de filtration glomérulaire estimé chez les personnes atteintes d'insuffisance rénale chronique [24]. Par conséquent, les modèles non gaussiens peuvent également avoir le potentiel de fournir des informations supplémentaires sur la microstructure du tissu rénal.
Bien que le modèle mono-exponentiel n'ait pas fourni le meilleur ajustement aux données DWI, cela ne signifie pas qu'il ne devrait pas être utilisé en clinique. Comme mentionné précédemment, l'ADC s'est avéré cliniquement utile dans la tumeur de Wilms [4-8]. De plus, ADC ne nécessite pas plusieurs valeurs b, ce qui est un avantage car de nombreux centres peuvent ne pas acquérir DWI avec plusieurs valeurs b en standard. Par conséquent, malgré la présente étude montrant un écart par rapport à une décroissance du signal mono-exponentielle, il est important de savoir que même si le modèle n'est peut-être pas le meilleur descripteur des données DWI, il est néanmoins cliniquement utile.
La méthode de sélection du modèle qui a fourni le meilleur ajustement est une faiblesse potentielle de cette étude. L'AIC prend en compte la complexité du modèle et la qualité de l'ajustement et semblait donc un choix approprié pour la comparaison et la sélection des modèles. Il est important de déterminer si un modèle est clairement le meilleur pour l'ensemble du tissu ou s'il n'y a qu'une petite différence entre les modèles. Ceci a été précédemment mis en évidence par Manikis et al. [25] dans le cancer du rectum, où bien que la mono exponentielle globale ait été préférée à l'IVIM, il y avait une forte hétérogénéité à travers le tissu. Cela a également été démontré dans les tumeurs de Wilms dans la présente étude, avec des modèles IVIM et exponentiels étirés démontrant de bons ajustements aux données. Dans cet esprit, il convient d'être prudent avant d'affirmer qu'un modèle particulier correspond le mieux aux données, car il se peut que de nombreux modèles soient presque égaux en qualité d'ajustement.

De plus, la valeur b maximale de 1000 s/mm² peut avoir été une limitation pour le modèle d'aplatissement car il devient plus sensible à des valeurs b plus élevées [26]. Par conséquent, avec une plage de valeurs b plus optimisée, ce modèle peut avoir obtenu de meilleurs résultats qu'avec les données actuelles. Cependant, dans une étude concernant la faisabilité du kurtosis dans les reins, un maximum de b=1000 s/mm' a également été utilisé [27]. De plus, la présente étude voulait se concentrer sur l'ajustement aux données cliniques acquises en routine qui n'ont pas de valeurs b extrêmement élevées. Ce sentiment a également été suggéré dans des travaux antérieurs qui comparaient le modèle mono-exponentiel à l'aplatissement dans le foie en utilisant également un maximum de b=1000 s/mm² 【28】.
Dans l'ensemble, cette étude a démontré que le modèle mono-exponentiel ne correspond pas aux données DWwI ainsi qu'aux données IVIM, exponentielle étirée ou aplatissement dans le tissu tumoral de Wilms ou le tissu rénal normal. De plus, il n'y avait pas de préférence de modèle pour
les sous-types cellulaires distincts. L'IVIM a fourni le meilleur ajustement pour le tissu rénal normal, et dans les tumeurs de Wilms, l'IVIM et les modèles exponentiels étirés ont fourni les meilleurs descripteurs des données. L'ADC est fréquemment utilisé dans la recherche clinique et, par conséquent, l'hypothèse est que le la décroissance du signal est monoexponentielle. Cependant, ces résultats suggèrent que dans la tumeur de Wilms et le tissu rénal normal, le signal DWI ne présente pas de décroissance mono-exponentielle. Par conséquent, l'utilisation d'autres modèles peut fournir des représentations plus précises de l'environnement tissulaire sous-jacent, et les paramètres dérivés peuvent fournir des informations cliniquement utiles.


Références
1. Pastore G, Znaor A, Spreafco F et al (2006) Incidence et survie des tumeurs rénales malignes chez les enfants européens (1978-1997): rapport du projet de système automatisé d'information sur le cancer infantile. Eur J Cancer 42:2103–2114. https://doi. org/10.1016/j.ejca.2006.05.010
2. van den Heuvel-Eibrink MM, Hol JA, Pritchard-Jones K et al (2017) Prise de position : Justification du traitement de la tumeur de Wilms dans le protocole UMBRELLA SIOP-RTSG 2016. Nature Rev Urol 14: 743–752. https://doi.org/10.1038/nrurol.2017.163
3. Vujanić GM, Sandstedt B, Harms D et al (2002) Classification de travail révisée de la Société internationale d'oncologie pédiatrique (SIOP) des tumeurs rénales de l'enfance. Med Pediatr Oncol 38: 79–82
4. Gawande RS, Gonzalez G, Messing S et al (2013) Rôle de l'imagerie pondérée en diffusion dans la différenciation des tumeurs abdominales pédiatriques bénignes et malignes. Pediatr Radiol 43:836–845. https://doi.org/10.1007/s00247-013-2626-0
5. Aslan M, Aslan A, Habibi HA et al (2017) IRM pondérée en diffusion pour différencier la tumeur de Wilms du neuroblastome. Diagn Interv Radiol 23:403–406. https://doi.org/10.5152/dir.2017.16541
6. Littooij AS, Humphries PD, Olsen ØE (2015) Variabilité intra et interobservateur des mesures du coefficient de diffusion apparent de la tumeur entière dans le néphroblastome : une étude pilote. Pediatr Radiol 45: 1651–1660. https://doi.org/10.1007/s00247-015-3354-4
7. Hales PW, Olsen ØE, Sebire NJ et al (2015) Un modèle multi-gaussien pour l'analyse de l'histogramme du coefficient de diffusion apparent du sous-type de tumeur de Wilms et de la réponse à la chimiothérapie. RMN Biomed 28:948–957. https://doi.org/10.1002/nbm.3337
8. Rogers HJ, Verhagen MV, Shelmerdine SC et al (2018) Une approche alternative à l'imagerie à contraste amélioré : l'imagerie pondérée par diffusion et l'imagerie pondérée T 1- identifient et quantifient la nécrose dans la tumeur de Wilms. Eur Radiol. https://doi. org/10.1007/s00330-018-5907-z
9. Le Bihan D, Breton E, Lallemand D et al (1988) Séparation de la difusion et de la perfusion dans l'imagerie IRM à mouvement incohérent intravoxel. Radiologie 168 : 497–505. https://doi.org/10.1148/radiologie.168.2.3393671
10. Bennett KM, Schmainda KM, Bennett RT et al (2003) Caractérisation des taux de diffusion de l'eau corticale distribués en continu avec un modèle exponentiel étiré. Magn Reson Med 50:727–734. https://doi.org/10.1002/mrm.10581
11. Jensen JH, Helpern JA, Ramani A et al (2005) Imagerie d'aplatissement diffusif : la quantification de la diffusion d'eau non gaussienne au moyen de l'imagerie par résonance magnétique. Magn Reson Med 53:1432–1440. https://doi.org/10.1002/mrm.20508
12. Zhang G, Wang S, Wen D et al (2016) Comparaison des modèles de diffusion non gaussiens et gaussiens de l'imagerie pondérée en diffusion du cancer du rectum à 3,0 T IRM. Sci Rep. https://doi. org/10.1038/srep38782
13. Reischauer C, Patzwahl R, Koh DM et al (2017) Analyse exponentielle non mono de l'imagerie pondérée par diffusion pour la surveillance du traitement dans les métastases osseuses du cancer de la prostate. Représentant Sci. https://doi.org/10.1038/s41598-017-06246-4
14. Winfield JM, deSouza NM, Priest AN et al (2015) Modélisation des données DW-MRI des tumeurs ovariennes primaires et métastatiques. Eur Radiol 25:2033–2040. https://doi.org/10.1007/s0033 0-014-3573-3
15. Pentang G, Lanzman RS, Heusch P et al (2014) Imagerie d'aplatissement de diffusion du rein humain : une étude de faisabilité. Magn Reson Imaging 32:413–420. https://doi.org/10.1016/j.mri.2014.01.006
16. Caroli A, Schneider M, Friedli I et al (2018) Imagerie par résonance magnétique pondérée en diffusion pour évaluer la pathologie rénale diffuse : une revue systématique et un document de déclaration. Nephrol Dial Transplant 33:ii29–ii40. https://doi.org/10.1093/ndt/gfy163
