partie 1 : effets anti-mélanogènes des vésicules extracellulaires dérivées des feuilles et des tiges des plantes dans les cellules de mélanome de souris et la peau humaine saine
Mar 23, 2023
Abstrait
L'intérêt des consommateurs pour les produits de l'industrie cosmétique à effet éclaircissant a accru la demande de préparations réduisant la mélanogénèse. Un certain nombre de médicaments anti-mélanogènes sont connus pour leurs effets secondaires, tels que la dermatite de contact et une toxicité élevée, et une mauvaise pénétration cutanée. Des recherches récentes considérables se sont concentrées sur les produits dérivés des plantes comme alternatives aux médicaments chimiothérapeutiques avec moins de conséquences secondaires.
Dans la présente étude, nous avons examiné l'action anti-mélanogénique des vésicules extracellulaires (VE) extraites du feuillage et des tiges du pathogène Dendropanax. En travaillant avec des méthodes spectrophotométriques et biochimiques, nous avons constaté que les vésicules extracellulaires dérivées des feuilles (LEV) et les vésicules extracellulaires dérivées de la tige (SEV) réduisaient la teneur en mélanine et l'activité de la tyrosinase (TYR) de manière dépendante de la concentration dans une lignée cellulaire de mélanome de souris B16BL6. L'analyse au microscope électronique a en outre démontré que les LEV et les SEV induisaient une diminution dépendante de la concentration de la teneur en mélanine dans les cellules de mélanome. Par rapport à l'arbutine comme contrôle positif, les LEV et les SEV ont montré un effet blanchissant plus fort sur les cellules de mélanome, et l'effet blanchissant des LEV était plus fort. Notamment, ni les LEV ni les SEV n'ont induit de cytotoxicité significative. Nous avons également examiné les effets des véhicules électriques d'origine végétale sur l'expression des protéines liées à la tyrosinase (TRP) dans les cellules de mélanome. Les LEV ont inhibé l'expression de gènes et de protéines liés à la mélanogenèse, notamment le facteur de transcription associé à la microphtalmie (MITF), TYR, TRP-1 et TRP-2. Dans un modèle d'épiderme humain, les LEV ont inhibé la mélanogénèse plus fortement que l'arbutine. Pris ensemble, nos données suggèrent que le lev des agents pathogènes D. pourrait être une nouvelle substance naturelle candidate à utiliser comme agent anti-mélanogène dans les préparations pharmaceutiques.
mots clés:VÉ d'origine végétale ; Les LEV etles SEV ; anti-mélanogène; Tyractivité; teneur en mélanine etBienfaits de l'extrait de cistanche

Introduction
La mélanine, une partie essentielle du système de pigmentation des cheveux, des yeux et de la peau humaine, est produite par les mélanocytes grâce à une procédure appelée mélanogenèse. Une accumulation aberrante de mélanine peut entraîner des troubles cutanés tels que des taches de rousseur, des taches de rousseur solaires et du mélasma, et peut également causer le cancer et le vitiligo. La régulation de la mélanogénèse est donc une stratégie essentielle dans le traitement des troubles hyperpigmentés. Par exemple, l'hydroquinone, un composé hydroxyphényle qui interfère avec l'activité TYR, est utilisée comme agent de blanchiment de la peau dans l'industrie cosmétique. Néanmoins, l'hydroquinone peut provoquer des effets secondaires tels que la dermatite de contact et la maladie de brunissement exogène. Va-acide est un autre agent synthétique qui inhibe l'activité TYR, mais son utilisation est associée à une fréquence élevée d'œdème ou d'irritation.
Il y a eu un intérêt croissant pour l'identification de médicaments alternatifs de sources naturelles contre la mélanogénèse, compte tenu des contraintes des composés chimiques existants, ce qui reflète le fait que les produits cosmétiques à base de plantes et d'herbes ont tendance à être plus doux, plus biodégradables et à présenter une toxicité plus faible que les synthétiques. composés. Il a été démontré que les extraits de feuilles de la maladie de Dendrobium inhibent la production de mélanine en interagissant directement avec l'activation intracellulaire de TYR et l'expression d'enzymes impliquées dans la biosynthèse de la mélanine. De la même manière, l'extrait de feuille de Croton officinalis a supprimé la teneur en mélanine et l'activité TYR cellulaire en inhibant le facteur de transcription lié à la mélanogénèse (MITF) et les enzymes mélanogènes. De plus, les feuilles de mûrier avaient un effet inhibiteur sur l'activité TYR et la formation de mélanine dans les cellules mélaniques-A. L'acide p-coumarique des feuilles de ginseng a été identifié comme le principal inhibiteur de TYR.

Herba Cistanche
Malgré le fait qu'une large gamme de composés botaniques a été utilisée dans les formulations cosmétiques médicinales, leur faible solubilité, leur faible affinité avec la cible et leur action éclaircissante modérée sur la peau ont entravé les progrès dans l'amélioration des effets thérapeutiques des cosmétiques botaniques. Cela a motivé la recherche de techniques nouvelles et progressives pour améliorer l'efficacité des composés médicinaux et bioactifs et améliorer leur efficacité de délivrance à la peau. Par exemple, un certain nombre de technologies de nano-livraison ont été développées avec succès, notamment la nano-belle pour des soins efficaces de la peau, la nano-quercétine pour retarder les dommages cellulaires causés par les rayons ultraviolets (UV), les nano-fullerènes pour la régénération du collagène et la prévention du vieillissement cutané. , la nano-lutéoline pour maintenir l'activité antioxydante et le nano-resvératrol pour protéger la peau des rayons UV.
Dans la présente étude, nous nous concentrons sur le rôle des vésicules extracellulaires d'origine végétale (VE). Des études récentes ont montré que les véhicules électriques dérivés de plantes ont une structure similaire à celle des exosomes isolés de mammifères et agissent comme des messagers extracellulaires médiant la communication intercellulaire. De plus, ces vésicules sont capables de transloquer l'ARNm, le micro-ARN (miARN), les lipides bioactifs et les protéines dans les cellules animales.
En attendant, nous avons étudié l'effet inhibiteur des VE dérivés de feuilles et de tiges de légumineuses malades sur la mélanogénèse. Nous avons caractérisé la taille et les propriétés des vésicules extracellulaires dérivées des feuilles (LEV) et des vésicules extracellulaires dérivées des tiges (SEV) extraites des feuilles et des tiges de légumineuses malades et avons montré que ces VE étaient facilement absorbées par les cellules de mélanome et n'étaient pas cytotoxiques. Pour démontrer les effets anti-mélanogènes des LEV et des SUV, nous avons examiné la teneur en mélanine et l'activité TYR dans les cellules de mélanome. Nous avons en outre évalué l'effet des véhicules électriques sur le processus complexe de synthèse de la mélanine en surveillant les changements dans les niveaux de diverses protéines et enzymes.
L'hormone de stabilisation des mélanocytes alpha (-MSH) se lie au récepteur de la mélanocortine 1 (MC1R) à la surface des cellules et active l'adénylate cyclase, entraînant une augmentation des niveaux intracellulaires d'adénosine monophosphate cyclique (AMPc). L'AMPc est médiée par la protéine kinase A dépendante de l'AMPc, conduisant à la phosphorylation de la protéine de liaison à l'élément de réponse à l'AMPc (CREB). Le CREB activé induit le MITF, qui est exprimé dans les mélanocytes et joue un rôle clé dans la différenciation et le développement des mélanocytes. -TRP1 est essentiel pour la translocation correcte de TYR vers la synthèse de mélanine et TRP2 joue un rôle important dans l'activité catalytique de TRP dans les premiers stades de la synthèse de mélanine. Ces trois éléments interagissent dans les cellules de mélanome (Fig. 1 supplémentaire).
Nous avons trouvé une expression réduite de MITF dans les cellules de mélanome traitées aux LEV, suivie d'une expression réduite de TYR, TRP -1 et TRP -2, et confirmé par microscopie électronique que la synthèse de mélanine était réduite dans ces cellules au niveau ultrastructural. Nous avons en outre confirmé l'effet anti-mélanogénique des LEV à l'aide d'un modèle épidermique humain reconstruit. Pour évaluer quantitativement l'effet inhibiteur des LEV sur la synthèse de mélanine cellulaire, nous avons préparé des solutions standard à partir de tissus et mesuré la teneur en mélanine à l'aide d'un colorimètre. les taches de mélanine ont été réduites dans les coupes de tissus colorées par Fontana-Masson. les LEV ont inhibé la production de mélanine plus efficacement que l'arbutine, un inhibiteur de TYR, qui a été utilisé comme témoin positif.
En résumé, ces résultats indiquent que l'utilisation de véhicules électriques dérivés de substances naturelles pour la gestion de l'hyperpigmentation est une approche future réalisable pour l'industrie pharmaceutique. De plus, avec les avantages d'une petite taille, d'une faible toxicité, d'une absorption élevée et de la sécurité environnementale, les véhicules électriques dérivés de plantes devraient être la prochaine génération de systèmes d'administration thérapeutique pour le traitement d'autres maladies. Notamment, les véhicules électriques dérivés de plantes ont de bons effets anti-mélanogènes sur les tissus cutanés humains reconstruits (similaires à l'épiderme humain), ouvrant la voie à de futurs essais cliniques.

Supplément Cistanche
Matériels et méthodes
1. Isolement des LEV et SUV de D. morbifera
Des feuilles et des tiges fraîches ont été récoltées sur l'île de Poge, Guandao-gun et Jeollanam-do. Les véhicules électriques ont été isolés à partir de 50 g de feuilles et de tige, respectivement, en broyant à l'aide d'un extracteur et en faisant passer le jus obtenu sur du papier filtre, puis en centrifugeant à 10 000 × g pendant 10 min. Les gros débris ont été éliminés en filtrant le surnageant à travers une membrane de 0,22 μm, suivi d'une centrifugation à l'aide d'un filtre centrifuge Amicon Ultra-4 PL 100 K (Merck Millipore. Darmstadt, Allemagne) pour concentrer les véhicules électriques en centrifugant les échantillons à 5000 × g pendant 10 min à 4 degrés. Après centrifugation, la concentration en protéines des véhicules électriques a été déterminée à l'aide d'un kit de dosage des protéines d'acide bis quinolinique (BCA) (Thermo Fisher Scientific, Waltham, MA, USA).
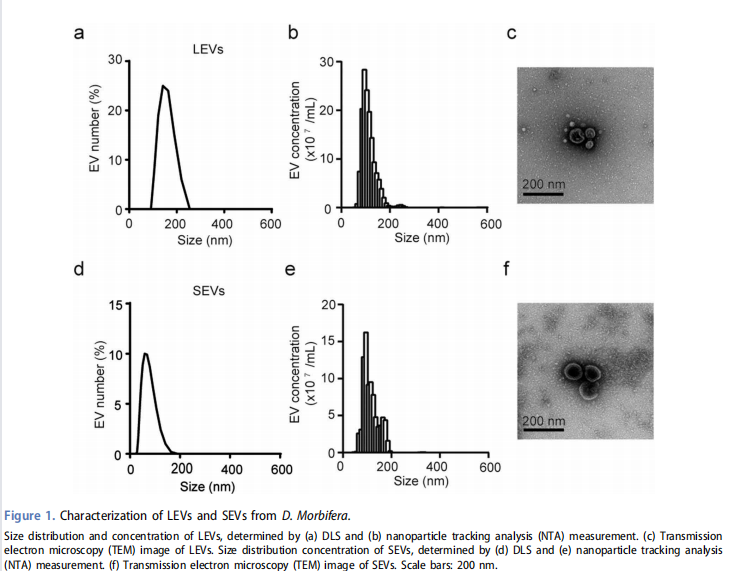
2. Caractérisation de la taille des véhicules électriques isolés
La taille hydrodynamique des véhicules électriques isolés a été mesurée par diffusion dynamique de la lumière (DLS), une technique utilisée pour déterminer la distribution de taille des petites particules en suspension, à l'aide d'un système Zetasizer Nano ZS90 (Malvern Instruments, Malvern, Royaume-Uni). Les véhicules électriques collectés ont été placés dans une cellule à température constante à 20 degrés. La distribution granulométrique et la moyenne z utilisées pour déterminer la distribution granulométrique hydrodynamique ont été déterminées en mesurant la fonction d'autocorrélation de l'intensité de diffusion. Les véhicules électriques isolés ont été dilués avec de l'eau à bulles sans vésicules, puis soumis à une analyse de suivi des nanoparticules (NTA) (Nanosight ; à l'aide d'un laser de 488 nm à 25 degrés).
3. Analyse par microscopie électronique à transmission des véhicules électriques
5 μL de solution d'échantillon ont été chargés sur un film de carbone recouvert d'une grille de cuivre pour une analyse par microscopie électronique à transmission (TEM). Après adsorption de l'échantillon pendant 1 min, les grilles ont été lavées avec une goutte d'eau pure puis colorées négativement avec 1 % d'acétate d'uranyle pendant 1 min. L'excès de tache a été enlevé avec du papier filtre et les grilles ont été séchées à l'air. Les échantillons ont été imagés au point entre 0.8 - 1.5 μm à l'aide d'un microscope électronique à transmission JEM- 1400 Plus (JEOL Ltd., Tokyo, Japon) équipé d'un pistolet Lab6 fonctionnant à 120 kV . Les images ont été enregistrées à l'aide d'une caméra CMOS UltraScan OneView (Gatan, Pleasanton, CA, USA).

Cistanche tubulosa
4. Préparation des liposomes
Les mélanges de liposomes ont été préparés en utilisant un rapport de 95:5 (mol/mol) de DMPC (1,2-stéaroyl-sn-glycérol-3-phosphocholine) (Avanti Polar Lipids, Alabaster, AL, USA) avec DSPE-mPEG (1,2-stéaroyl-sn-glycérol-3-phosphoéthanolamine-[méthoxy(polyéthylène glycol)- 2000] (lipides polaires Avanti) pour préparer les mélanges de liposomes sous forme de membranes lipidiques. le colorant fluorescent hydrophobe 1,1-dioctadécyl-3,3,3ʹ,3ʹ-tétraméthylindocarbocyanine perchlorate (DiI, Invitrogen, Waltham, MA, USA) a été mélangé avec des véhicules électriques, 725,49 ug de DMPC, 151,64 ug de DSPE-PEG et 15 ug DiI. Après évaporation du solvant organique, la membrane contenant le mélange lipide et DiI a été hydratée avec 1 ml de solution saline tamponnée au phosphate (PBS). Ensuite, des liposomes de 100 nm ont été préparés à l'aide d'une extrudeuse (Avanti Polar Lipides).
5. Essais de culture cellulaire et de viabilité
Des cellules de mélanome B16BL6 ont été cultivées dans un milieu essentiel alpha-minimal (alpha-MEM) contenant 10 % de sérum bovin fœtal (Rocky Mountain Biologicals, Missoula, MT, États-Unis) et 1 % de pénicilline/streptomycine (Lonza, Bâle, Suisse) (Gibco, Thermo Fisher Scientific) en culture. Les cellules ont été incubées à 37 degrés dans une atmosphère humidifiée à 5 % de CO2. 100 μL de cellules de mélanome B16BL6 ont été inoculés dans des plaques à puits 96- (5 × 104 cellules/puits) pour des tests de viabilité cellulaire. Après incubation pendant 24 h, les cellules ont été traitées avec des LEV et des SEV à des concentrations de 1, 5 et 10 µg/mL, respectivement, pendant 24 h. Les concentrations de liposomes et d'arbutine étaient de 10 µg/mL et 70 µg/mL, respectivement, pour toutes les expériences. 10 µL de réactif EZ-Cytox (Daeil Lab Service, Séoul, Corée) ont ensuite été ajoutés dans chaque puits. Les plaques ont été incubées pendant 1 h. Les plaques ont ensuite été doucement agitées et l'absorbance a ensuite été mesurée à 450 nm à l'aide d'un marqueur enzymatique (BioTek, Winooski, VT, USA).
LES RÉFÉRENCES
[1] Meredith P, Sarna T. Les propriétés physiques et chimiques de l'eumélanine. Pigment Cell Res. 2006;19(6):572–594.
[2] Grimes PE. Mélasma : considérations étiologiques et thérapeutiques. Arche Dermatol. 1995;131(12):1453–1457.
[3] Todd MM, Rallis TM, Gerwels JW, et al. Une comparaison de 3 lasers et de l'azote liquide dans le traitement des lentigos solaires : un essai comparatif randomisé, contrôlé. Arche Dermatol. 2000;136(7):841–846.
[4] Kawalek AZ, Spencer JM, Phelps RG. Laser excimer combiné et tacrolimus topique pour le traitement du vitiligo : une étude pilote. Chirurgie Dermatol. 2004;30(2):130–135.
[5] Bastiaens M, Ter Huurne J, Gruis N, et al. Le gène du récepteur de la mélanocortine-1-est le principal gène des taches de rousseur. Hum Mol Genet. 2001;10(16):1701–1708.
[6] Pillaiyar T, Manickam M, Jung SH. Régulation à la baisse de la mélanogénèse : découverte de médicaments et options thérapeutiques. Drug Discov aujourd'hui. 2017;22(2):282–298.
[7] Hu ZM, Zhou Q, Lei TC, et al. Effets de l'hydroquinone et de ses dérivés glucosides sur la mélanogénèse et l'anti-oxydation : biosécurité en tant qu'agents de blanchiment de la peau. J Dermatol Sci. 2009;55(3):179–184.
[8] Westerhof W, Kooyers T. Hydroquinone et ses analogues en dermatologie - un risque potentiel pour la santé. J Cosmet Dermatol. 2005;4(2):55–59.
[9] Picardo M, Carrera M. Traitements nouveaux et expérimentaux du chloasma et d'une autre hypomélanose. Dermatol Clin. 2007;25(3):353–362.
[10] Shin JW, Park KC. Utilisation clinique actuelle des agents dépigmentants. Dermatol Péché. 2014;32(4):205–210.
[11] Chaita E, Lambrinidis G, Cheimonidi C, et al. Propriétés anti-mélanogènes des plantes grecques. Un nouvel agent dépigmentant du bois de Morus alba. Molécules. 2017;22(4):1–14.
[12] Park SA, Park J, Park CI, et al. Activité antioxydante cellulaire et effets blanchissants des extraits de feuilles de Dendropanax morbifera. Microbiol Biotechnol Lett. 2013;41(4):407–415.
[13] Chatatikun M, Yamauchi T, Yamasaki K, et al. Effet anti-mélanogénique des feuilles de Croton roxburghii et Croton sublyratus dans les cellules B16F10 stimulées par la MSH. J Tradit Complément Med. 2019;9(1):66–72.
[14] Lee SH, Choi SY, Kim H, et al. Le mulberroside F isolé des feuilles de Morus alba inhibe la biosynthèse de la mélanine. Biol Pharma Bull. 2002;25(8):1045–1048.
[15] Lim JY, Ishiguro K, Kubo I. Acide P-coumarique inhibiteur de la tyrosinase des feuilles de ginseng. Phytother Res. 1999;13(5):371–375.
[16] Chanchal D, Swarnlata S. Nouvelles approches dans les cosmétiques à base de plantes. J Cosmet Dermatol. 2008;7(2):89–95.
[17] Ganesan P, Choi DK. Application actuelle des nano-cosméceutiques à base de phytocomposés pour la beauté et la thérapie de la peau. Int J Nanomédecine. 2016;11 (11):1987–2007.
[18] Takahashi M, Kitamoto D, Asikin Y, et al. Les liposomes encapsulant l'extrait de gel de feuille d'Aloe vera améliorent considérablement la prolifération et la synthèse de collagène dans les lignées cellulaires de la peau humaine. J Oleo Sci. 2009;58(12):643–650.
[19] Bose S, Du Y, Takhistov P, et al. Optimisation de la formulation et administration topique de quercétine à partir de nanosystèmes à base de lipides solides. Int J Pharm. 2013;441(30):56–66.
[20] Ngan CL, Basri M, Tripathy M, et al. Intervention cutanée de la nanoémulsion intégrée au fullerène dans la régénération structurelle et du collagène contre le vieillissement cutané. Eur J Pharm Sci. 2015;70(5):22–28.
[21] Mitri K, Shegokar R, Gohla S, et al. Nanoporteurs lipidiques pour l'administration cutanée de lutéine : préparation, caractérisation, stabilité et performance. Int J Pharm. 2011;414 (1–2):267–275.
[22] Juškaitė V, Ramanauskienė K, Briedis V. Conception et formulation de microémulsions optimisées pour l'administration cutanée de resvératrol. Evid Based Complement Alternat Med. 2015 ; 2015 : 1–10.
[23] Zhang M, Viennois E, Xu C, et al. Les nanoparticules comestibles d'origine végétale comme nouvelle approche thérapeutique contre les maladies. Barrières tissulaires. 2016;4(2):1–9.
[24] Criton M, Le Mellay-Hamon V. Analogues de N-hydroxy-N′-phénylthiourée et N-hydroxy-N′-phénylurée comme inhibiteurs de la formation de tyrosinase et de mélanine. Bioorg Med Chem Lett. 2008;18 (12):3607–3610.
[25] Kobayashi T, Audience VJ. Interaction directe de la tyrosinase avec Tyrp1 pour former des complexes hétérodimères in vivo. J Cell Sci. 2007;120(24):4261–4268.
[26] D'Mello S, Finlay G, Baguley B, et al. Voies de signalisation dans la mélanogénèse. Int J Mol Sci. 2016;17(7):1–18.
[27] Fang D, Tsuji Y, Setaluri V. Régulation négative sélective du gène de la famille des tyrosinases TYRP1 par inhibition de l'activité du facteur de transcription des mélanocytes, MITF. Nucleic Acids Res. 2002;30(14):3096–3106.
[28] Oh MJ, Hamid MA, Ngadiran S, et al. L'extrait de Ficus deltoidea (Mas cotek) a exercé une activité anti-mélanogénique en empêchant l'activité de la tyrosinase in vitro et en supprimant l'expression du gène de la tyrosinase dans les cellules de mélanome B16F1. Arch Dermatol Res. 2011;303(3):161–170.
[29] Jang EJ, Shin Y, Park HJ, et al. L'activité anti-mélanogénique de la phytosphingosine via la modulation de la voie de signalisation du facteur de transcription associé à la microphtalmie. J Dermatol Sci. 2017;87(1):19–28.
[30] Toyofuku K, Wada I, Valencia JC, et al. Les albinismes oculocutanés de types 1 et 3 sont des maladies de rétention du RE : la mutation de la tyrosinase ou de Tyrp1 peut affecter le traitement des protéines mutantes et de type sauvage. Faseb J. 2001;15:2149–2161.
[31] Xue L, Li Y, Zhao B, et al. TRP-2 médie la pigmentation de la couleur du pelage dans la peau de mouton. Mol Med Rep. 2018;17:5869–5877.
[32] Mu J, Zhuang X, Wang Q, et al. Communication interspécifique entre les cellules hôtes de l'intestin des plantes et des souris par le biais de nanoparticules de type exosome dérivées de plantes comestibles. Mol Nutr Food Res. 2014;58(7):1561–1573.






