La déplétion à long terme des lymphocytes B est associée à la régénération de la fonction rénale
Mar 17, 2022
Contact:joanna.jia@wecistanche.com/ Whatsapp : 008618081934791
Susanne V. Fleig, et al
Résumé
Arrière plan:Chroniqueun reinmaladie(IRC) est une affection courante qui augmente la mortalité et le risque de morbidités cardiovasculaires et autres, quelle que soit l'affection rénale sous-jacente. L'inflammation chronique favorise la fibrose rénale. Récemment, des infiltrats de lymphocytes B rénaux ont été décrits dans la maladie rénale chronique d'étiologies diverses au-delà de l'auto-immunité.
Méthodes :Nous avons ici étudié les lymphocytes B et les indicateurs de formation de structure lymphoïde tertiaire dans les biopsies rénales humaines. La fonction rénale a été étudiée pendant la déplétion à long terme des cellules B chez des patients humains atteints de néphropathie membraneuse et d'IRC d'origine inconnue.
Résultats:Des profils de cytokines de la formation de structures lymphoïdes tertiaires ont été détectés dans l'interstitium rénal humain dans une gamme deun reinmaladies. Des structures complexes de cellules B compatibles avec la formation d'organes lymphoïdes tertiaires ont été mises en évidence dans la néphropathie membraneuse humaine. Ici, la densité des lymphocytes B n'était pas associée de manière significative à la sévérité de la protéinurie, mais à une fonction rénale excrétrice moins bonne. En revanche, la récupération des excréteursun reinfonctionn'a été observé qu'après 18 mois de traitement continu, ce qui correspond à un processus structurel. Des structures lymphatiques tertiaires rénales ont également été détectées en l'absence deun reinmaladie. Pour commencer à déterminer si la déplétion des lymphocytes B peut affecter l'IRC dans une population plus large, nous avons évaluéun reinamusementction chez les patients neurologiques atteints d'IRC (Chroniqueun reinmaladie)d'origine inconnue. Dans cette cohorte, l'eGFR a augmenté de manière significative dans les 24 mois suivant la déplétion des lymphocytes B.
Conclusion:Épuisement à long terme des lymphocytes B associé à une amélioration significative de l'excrétionun reinfonctiondans la MRC humaine (Chroniqueun reinmaladie). La cinétique et les mécanismes de l'agrégation des lymphocytes B rénaux devraient être étudiés plus avant pour stratifier l'impact des lymphocytes B et de leurs agrégats en tant que cibles thérapeutiques.
MOTS CLÉS:cancer, migration cellulaire, foie/hépatocytes
Cistanche peut s'améliorerfonction rénale
1 | INTRODUCTION
Les lymphocytes B peuvent infiltrer directement les organes non lymphoïdes, y compris le rein. Une inflammation persistante peut induire des structures organisées, qui contiennent des lymphocytes T et des vaisseaux lymphatiques et sont conformes à la définition des structures lymphoïdes tertiaires (TLS).1,2 Les TLS ressemblent aux ganglions lymphatiques dans la composition et l'architecture des cellules, mais sont confinés par l'organe hôte et déplacent le parenchyme de l'organe. Les lymphocytes B sont recrutés par la chimiokine locale exprimée dans le stroma CXCL13 (nom alternatif : attractif des lymphocytes B 1)1–3. Ils sécrètent à leur tour des lymphotoxines, notamment la lymphotoxine B(LTB),4 qui favorisent la différenciation du stroma périvasculaire en cellules réticulaires fibroblastiques du tissu lymphoïde et en cellules dendritiques folliculaires. cellules,5,6 consolidant ainsi la nouvelle structure lymphoïde.7
Dans le rein, le SLT a été signalé dans une gamme de maladies auto-immunes, notamment la glomérulonéphrite associée aux ANCA, le lupus érythémateux disséminé rénal, la glomérulopathie membraneuse et l'IgAnéphrite.8–12 .13–16 Plus récemment, des TLS rénaux ont été décrits en l'absence de stimulus anallo-immun, par exemple lors du suivi à long terme d'une lésion d'ischémie‐reperfusion murine1,16 et de pyélonéphrite humaine sévère.17
La déplétion thérapeutique des lymphocytes B est cliniquement couronnée de succès dans une gamme deun reinmaladiesy compris le rejet d'allogreffe rénale et les phritides glomérulaires. Par exemple, dans la néphropathie membraneuse, une cause fréquente du syndrome néphrotique, la déplétion des lymphocytes B par le rituximab permet d'obtenir des taux de rémission similaires à ceux des protocoles précédents tels que le régime de Ponticelli et les inhibiteurs de la calcineurine.18–20 Les preuves actuelles comprennent plusieurs essais contrôlés21,22 ainsi qu'une gamme série de cas. Actuellement, la déplétion des anticorps auto-oraux et, par conséquent, l'abrogation de l'activation immunitaire innée en aval et la destruction des tissus sont considérées comme le principal mécanisme d'action. La déplétion des lymphocytes B par le rituximab a également dissous les infiltrats diffus de lymphocytes B dans les allogreffes rénales humaines,14 tandis que la déplétion des lymphocytes B à court terme était apparemment inefficace pour la dissolution du TLS, bien que chez un nombre très limité de patients.23 thérapie de déplétion cellulaire.24
Il est concevable que les infiltrats diffus de lymphocytes B et le TLS puissent altérer la fonction des organes même en l'absence d'immunité médiée par les anticorps. Si le TLS rénal se forme inchroniqueun reinmaladie(CKD) d'étiologies diverses, la déplétion à long terme des lymphocytes B devrait également bénéficier aux patients sans diagnostic d'insuffisance rénale médiée par les anticorps. Nous avons étudié ici l'infiltration des lymphocytes B et les marqueurs de la formation de TLS dans la glomérulonéphrite humaine et évalué le développement deun reinfonctionau cours de la déplétion à long terme des lymphocytes B dans la glomérulonéphrite membraneuse et l'IRC d'origine inconnue.
2|MATÉRIEL ET MÉTHODES
2.1|Populations étudiées
Les analyses de données ont été réalisées après l'approbation du comité d'éthique (MHH 2018‐8172 et 2019‐8275) conformément à la déclaration d'Helsinki. Dans le service de néphrologie, les patients présentant un diagnostic histologique de glomérulopathie membraneuse ont été identifiés à partir des dossiers électroniques utilisant les codes de facturation des patients hospitalisés « glomérulonéphrite membraneuse » et « syndrome néphrotique dû à la néphropathie membraneuse » 2015-2019 et à partir des dossiers des cliniques externes spécialisées en néphrologie. L'absence de suivi plus long parmi les répondeurs était due au début récent du traitement (n=6), à la perte de suivi (n=3), au manque de données de suivi pour le mois 18 (avec une bonne réponse au mois 24, n=1), et le début de l'hémodialyse (n=1). Au moins une mesure des lymphocytes B a été effectuée chez chaque patient après la déplétion des lymphocytes B et celles-ci étaient négatives. Les patients présentant des résultats de biopsie rénale indiquant une vascularite ont été exclus (n=2). Sur 65 patients identifiés, 13 avaient un débit de filtration glomérulaire estimé (DFGe) de 70 ml/min/1,73 m2 ou moins au début du traitement et ont été inclus dans cette analyse.
Les valeurs de laboratoire obtenues à la Hannover MedicalSchool ont été enregistrées avant le début du rituximab et aux intervalles indiqués par la suite. L'eGFR a été calculé à l'aide duUn reinMaladieSelon la formule de l'Epidemiology Collaboration (CKD‐EPI), 25 les protéinuries ont été mesurées par analyse de bandelettes réactives dans la cohorte de neurologie et en tant que rapport protéine/créatinine dans des échantillons d'urine ponctuels chez les patients néphrologiques.

Cistanche peut s'améliorerfonction rénale
2.2|Analyse des données de la matrice de gènes
L'expression de la LTB tubulo-interstitielle et de CXCL13 a été analysée dans des ensembles de données publiques de la cohorte européenne de la banque d'ADNc, du Nephrotic Syndrome Study Network et du Vasculitis Clinical Research Consortium26 obtenus au NCBI (GSE104948 et GSE104954).
2.3|Immunomarquage, analyse confocale et quantification de l'infiltrat de lymphocytes B dans la glomérulopathie membraneuse
Dans toutes les biopsies disponibles et un échantillon de néphrectomie d'un patient atteint d'oxalose, une immunocoloration avec anti‐CD20 (1:50 ; clone L26 ; Agilent) de coupes de biopsie rénale de 3 µm déparaffinées et réhydratées incluses dans la paraffine a été menée pendant 90 min après la récupération de l'épitope induite par la chaleur avec un tampon d'acide T‐éthylènediamine tétra‐acétique (pH 9,0, Zytomed Systems), une activité de peroxydase endogène (3% H2O2) et un blocage des protéines (Zytomed). Des contrôles négatifs omettant les anticorps primaires ont été inclus dans tous les protocoles de coloration. Pour la détection, le système polymère de peroxydase de raifort ZytoChem Plus (souris/lapin; Zytomed) a été utilisé avant le chromogène 3,3ʹ-diaminobenzidine (Zytomed) et la contre-coloration par l'hémalum. Les lames à fond clair colorées pour CD20 ont été numérisées à un grossissement original de 40 × (Aperio CS2, LeicaMicrosystems). La zone immunocolorée a été quantifiée dans une approche basée sur les pixels avec un seuil défini de manière interactive à l'aide d'une plateforme d'analyse d'images open source (QuPath, version 0.1.2, https://qupath.github.io/).27 Le même seuil a été utilisé pour tous sections. Chaque section a été contrôlée pour la qualité de la coloration, le seuil et l'exactitude des annotations par deux pathologistes en aveugle pour la coloration, le diagnostic et le cas. Les artefacts (par exemple, les plis tissulaires, les irrégularités chromogènes) ont été exclus de l'analyse. Les groupes ont été divisés par des densités de lymphocytes B supérieures et inférieures à la médiane au début du traitement.
Des échantillons sélectionnés ont été colorés pour l'imagerie confocale à l'aide d'un anti-AF488 de chèvre secondaire (Invitrogen) et d'un anti-SMA conjugué à Cy3 (1A3, Sigma). Le contre-colorant nucléaire au 4,6-diamidino-2-phénylindole (DAPI, Invitrogen) a été appliqué et les lames ont été montées dans un milieu de montage Immunoselectantifading (Dianova). Les images ont été obtenues avec un microscope laser confocal Leica TCS SP8 et un objectif multi‐immersion 20× (Leica). L'analyse a été réalisée avec NIH ImageJ et GIMP (version 2.8)
2.4|Statistiques
L'analyse statistique a été réalisée à l'aide de Prism 8. Les données sont exprimées en moyenne ± SEM. Le test de distribution gaussienne a été réalisé à l'aide du test de D'Agostino et Pearson. Deux variables ont été comparées à l'aide de tests t ou du test de Kruskal-Wallis pour les échantillons non distribués normalement. Des comparaisons multiples ont été effectuées en utilisant une ANOVA à un facteur avec les tests de comparaisons multiples de Dunn ou de Dunnett, comme indiqué. La régression multivariée a été effectuée à l'aide de SAS 9.4 (SAS Institute). Les valeurs de p inférieures à 0,05 ont été considérées comme significatives, les valeurs de p sont indiquées comme suit :*p < 0,05,="" **p="">< 0,01,="" ***p=""><>
3|RÉSULTATS
3.1|Infiltrats de cellules B et médiateurs de l'organisation du tissu lymphoïde dans les maladies rénales humaines
L'immunomarquage pour le marqueur de lymphocytes B CD20 et le marqueur structurel SMA a été évalué dans des biopsies rénales humaines avec néphropathie membraneuse (Figure 1A). Confirmant les découvertes antérieures d'infiltrats de lymphocytes B,9,10, il a en outre révélé des structures organisées, conformes à la définition du TLS.
Pour traiter un plus large éventail de maladies rénales, les médiateurs de la formation de TLS CXCL131,8 et la lymphotoxine B (LTB)7,9 dans l'interstitium rénal ont été analysés dans des ensembles de données d'expression génique provenant de 195 biopsies humaines (Figure 1B, C26). Comme on pouvait s'y attendre, les deux ont augmenté dans des conditions hautement inflammatoires telles que la glomérulonéphrite en croissant, le lupus érythémateux disséminé rénal et la néphropathie à IgA par rapport aux reins sains de donneurs d'organes vivants. En outre, il y a également eu une augmentation significative des maladies plus chroniques, notamment la néphropathie diabétique et la glomérulopathie membraneuse.
Ces mesures sont cohérentes avec la présence de structures lymphoïdes tertiaires chez l'homme.un reinmaladie, à savoir la glomérulopathie membraneuse.

3.2|Les infiltrats de lymphocytes B dans la glomérulopathie membraneuse s'associent à une diminution de la fonction rénale excrétrice
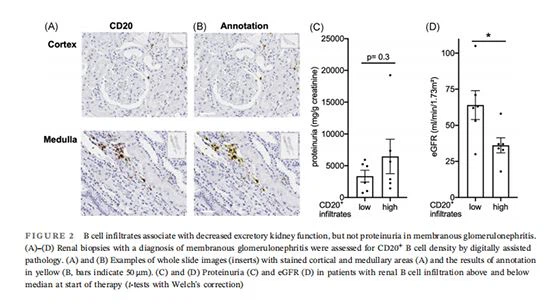
Pour étudier la pertinence fonctionnelle des infiltrats de lymphocytes B dans la néphropathie membraneuse, nous avons évalué leur étendue par analyse d'image assistée numériquement (Figure 2A, B). Les patients ont été divisés en fonction de l'abondance de l'infiltrat de lymphocytes B au début de la thérapie de déplétion des lymphocytes B. La protéinurie, une manifestation majeure de la glomérulopathie membraneuse, ne différait pas significativement entre les groupes (Figure 2C), au nord du stade de la glomérulopathie membraneuse (2,1 ± 0.8 vs.2,5 ± 0.7, p{{10 }} .3, test de Mann–Whitney). Cependant, des infiltrats de lymphocytes B plus abondants dans le tissu rénal sont associés à une aggravation significative de l'excrétion.un reinfonction(Figure 2D).
Ceci suggère l'hypothèse que les infiltrats de lymphocytes B peuvent être fonctionnellement pertinents au-delà de l'induction de la protéinurie.

Cistanche peut s'améliorerfonction rénale
3.3|Effet de la déplétion à long terme des lymphocytes B dans la glomérulopathie membraneuse
Nous avons ensuite étudié les conséquences fonctionnelles de la déplétion à long terme des lymphocytes B dans cette cohorte de néphropathies membraneuses. 15 ml/min/1,73 m2 et ont été inclus dans cette analyse. Comme dans les rapports précédents, 80 % ont réduit leur protéinurie de plus de 25 % dans les 12 mois suivant la première administration de rituximab et ont été classés comme répondeurs selon la définition de l'essai MENTOR21 (tableau 1). La diminution de la protéinurie chez les répondeurs était détectable après 6 mois d'épuisement des lymphocytes B (figure 3A).

Si l'accumulation de lymphocytes B est pertinente sur le plan physiopathologique, la déplétion à long terme devrait améliorer le DFGe au-delà des effets sur la protéinurie. En effet,fonction rénalequantifié par eGFR amélioré, mais n'a atteint la signification qu'après 18 mois (Figure 3B). Nous avons en outre abordé les facteurs cliniques susceptibles d'affecter la récupération fonctionnelle rénale. Le sevrage des inhibiteurs de la calcineurine peut améliorer l'eGFR et ces médicaments ont été prescrits à 54 % de notre cohorte à différents moments avant l'administration du rituximab. Cependant, cette thérapie n'a pas été significativement associée à la récupération de la fonction rénale excrétrice (tableau 2). Le retard marqué dans l'amélioration de l'eGFR plaide également contre les effets hémodynamiques.
Immunosuppression antérieure et âge, à la fois au moment du diagnostic et lors de la première déplétion en lymphocytes B, négativement associés à la récupération rénale. L'amélioration de l'eGFR est significativement inversement corrélée à l'âge au moment du diagnostic (Figure 3C). L'âge et les traitements antérieurs, mais pas le délai entre le diagnostic et la déplétion des lymphocytes B, sont restés un facteur significatif dans l'analyse de régression linéaire multivariée (tableau 3).
Ces résultats démontrent une amélioration fonctionnelle avec une déplétion à long terme des lymphocytes B pour la glomérulopathie membraneuse chez l'homme.





3.4|Amélioration de la fonction rénale avec déplétion à long terme des lymphocytes B dans l'IRC d'origine inconnue
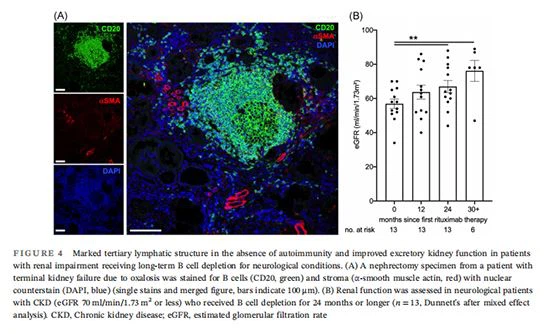
Des infiltrats de cellules B ont été trouvés dans une variété d'affections rénales au-delà de la néphropathie membraneuse. À titre d'exemple de non médiée principalement par les anticorpsun rein maladie, nous avons détecté un grand organe lymphoïde tertiaire comprenant un centre agerminal dans un spécimen de néphrectomie d'un patient présentant une oxalose (Figure 4A). Si elles sont fonctionnellement pertinentes, leur suppression devrait être bénéfique au-delà d'une maladie auto-immune bien définie.
Pour commencer à aborder cette hypothèse, nous avons étudié des patients hospitalisés eGFR recevant une déplétion chronique en lymphocytes B pour des conditions neurologiques avec un eGFR de 70 ml/min/1,73 m2 ou moins. Comme détaillé dans les méthodes, les patients avec un diagnostic formel de maladie rénale, à savoir la glomérulonéphrite, ont été exclus. Les caractéristiques cliniques et de laboratoire sont présentées dans le tableau 4. Le DFGe a augmenté de manière significative après deux ans de traitement (figure 4B). L'augmentation est très probablement même sous-estimée en raison de l'amélioration de la fonction neurologique et de la masse musculaire.
Ces données suggèrent que la déplétion chronique des lymphocytes B pourrait conférer un effet bénéfique dans l'IRC (Chroniqueun reinmaladie)indépendante d'une entité pathologique spécifique.


Cistanche peut s'améliorerfonction rénale
4|DISCUSSION
Nos données démontrent une amélioration deun reinfonctionavec une déplétion à long terme des lymphocytes B. Étant donné que les infiltrats de lymphocytes B organisés se développent dans une gamme de maladies rénales d'étiologies diverses, ces résultats encouragent leur investigation plus poussée en tant que cibles thérapeutiques au-delà des maladies auto-immunes.
Dans la glomérulopathie membraneuse, nous avons observé une amélioration de l'excrétionun reinfonctionaprès 18 mois de déplétion en lymphocytes B. Cela concorde avec d'autres rapports.28–31 Une amélioration du NoeGFR a été rapportée chez les participants traités au rituximab de l'essai MENTOR.21 Cependant, ces patients ont subi leur dernière déplétion en lymphocytes B au cours du 6ème mois de l'étude. Des considérations similaires s'appliquent à l'étude GEMRI TUX, qui a rapporté une fonction rénale excrétrice stable après 6 mois22 et à la dose unique de rituximab administrée dans l'étude STARMEN.32 Cela souligne la nécessité d'observations prolongées du succès thérapeutique dans la néphropathie membraneuse après déplétion des lymphocytes B. Nos données de patients atteints d'IRC (Chroniqueun reinmaladie)d'origine inconnue proposent que cela puisse également s'appliquer à d'autres formes de maladie rénale, comme le suggèrent les modèles expérimentaux murins.16 Cela concorde avec la régulation à la hausse significative de l'expression du gène TLS, ainsi que la RPGN inhumaine, la néphropathie à IgA et la néphropathie diabétique trouvées dans notre analyse. Une meilleure compréhension des mécanismes de formation des TLS, y compris l'interaction avec les vaisseaux sanguins et les signaux spécifiques aux organes1,9,16, est nécessaire pour étendre les approches thérapeutiques au-delà de la déplétion des lymphocytes B.
Les schémas thérapeutiques dans la néphropathie membraneuse se sont développés rapidement ces dernières années.20,33 Le taux de réponse de la protéinurie dans notre cohorte de soins tertiaires correspond à des rapports similaires28,29,34 et était plus élevé que chez d'autres, qui ont reçu des doses plus faibles de rituximab.30,35 En accord avec les précédents études, aucune caractéristique clinique n'est associée à la réponse de protéinurie au rituximab. Il est important de noter que, comme dans la plupart36 mais pas dans tous les rapports,35 un DFGe inférieur n'a pas eu d'effet négatif sur la réponse de la protéinurie, à un âge avancé.37 Notre présente analyse est limitée par des mesures PLA2R incomplètes, qui ont été associées à la réponse de la protéinurie dans la glomérulonéphrite membraneuse.22,35,38 Les médicaments concomitants, y compris les corticostéroïdes, qui sont également administrés avec les perfusions de rituximabine, peuvent avoir influencé la réponse. L'arrêt des inhibiteurs de la calcineurine peut améliorer de manière aiguë la fonction rénale, comme indiqué pour la néphropathie membraneuse dans l'essai MENTOR et d'autres.21,31,39 Les inhibiteurs de la calcineurine font également partie des approches immunosuppressives combinées dans la néphropathie membraneuse sévère.31,32 Il est rassurant qu'ils n'aient pas empêché la récupération rénale à long terme chez les patients de notre cohorte. Collectivement, nos observations renforcent encore la preuve d'une réduction efficace de la protéinurie et d'un faible taux d'événements indésirables au cours de la déplétion des lymphocytes B pour la glomérulopathie membraneuse primaire.
Le vieillissement a affecté négativement la régénération rénale dans un certain nombre d'études expérimentales et cliniques.42–44 Les reins biologiquement âgés sont mis au défi de fournir suffisamment de divisions cellulaires pour la régénération fonctionnelle. De plus, un vieillissement glomérulaire accru a été décrit dans les maladies glomérulaires, y compris la glomérulopathie membraneuse.42,45 Bien que nous ne sachions pas qu'une corrélation négative entre l'âge et la régénération ait été rapportée précédemment dans la glomérulopathie membraneuse, nos données concordent avec les résultats des patients atteints du syndrome néphrotique dû à d'autres étiologies, y compris une maladie modifiée minimale et une glomérulosclérose focale et segmentaire.46 Ici, une amélioration de l'eGFR a été observée après 1 an de déplétion des lymphocytes B exclusivement chez les patients plus jeunes, principalement les enfants. Nos données plaident en faveur d'un facteur dépendant de l'âge dans la régénération après un traitement réussi également dans la glomérulopathie membraneuse. Notre cohorte de répondeurs comprenait des patients âgés de 28 à 73 ans au moment du diagnostic et de 33 à 77 ans au premier traitement par le rituximab, avec un délai entre le diagnostic et la déplétion en lymphocytes B de 0–318 mois (moyenne de 77 mois). Ces valeurs sont attendues fortement corrélées. La large tranche d'âge nous a permis de commencer à explorer si un retard dans le traitement contribuait à l'amélioration de l'eGFR avec facultés affaiblies. Nos données n'indiquent pas d'effet délétère du retard du traitement par le rituximab.
Notre étude est également limitée par le fait qu'il y avait trop peu de patients avec du matériel de biopsie pour la coloration des lymphocytes B et un suivi à long terme pour une association quantitative avec l'étendue de la réponse eGFR (n=7). Nous avons utilisé la quantification assistée par ordinateur de l'ensemble de la lame pour obtenir un maximum d'informations sur l'abondance des lymphocytes B dans le rein. Cependant, compte tenu de leur nature dispersée, même un noyau de biopsie complet peut ne pas refléter l'étendue totale.
En résumé, nos données proposent une justification supplémentaire pour l'utilisation de la déplétion à long terme des lymphocytes B dansun reinmaladiespar perturbation des structures locales dominées par les lymphocytes B. Des essais contrôlés étendus comprenant des évaluations histologiques en série sont nécessaires pour valider cette approche. Nos résultats peuvent encourager une analyse systématique du développement de la fonction rénale dans des cohortes supplémentaires.
REMERCIEMENTS
Nous reconnaissons le soutien de la préparation des données de la matrice ingénique de la génomique de l'unité centrale du MHH et de la microscopie laser de l'unité centrale, D. Kijas et E. Christians avec immunocoloration. SvV était soutenu par la Deutsche Forschungsgemeinschaft.
LES CONTRIBUTIONS DE L'AUTEUR
Susanne V. Fleig, Christoph Schröder, Hermann Haller, Thomas Skripuletz et Sibylle von Vietinghoff ont conçu la recherche. Susanne V. Fleig, Franz Felix Konen, ChristophSchröder, Jessica Schmitz, Stefan Gingele, Jan HinrichBräsen et Svjetlana Lovric ont acquis des données. Franz FelixKonen, Christoph Schröder, BMWS et Sibylle vonVietinghoff ont analysé les données. Susanne V. Fleig, Franz FelixKonen, Christoph Schröder et Sibylle von Vietinghoff ont écrit le manuscrit avec l'aide de tous les coauteurs, tous les auteurs ont lu et approuvé le manuscrit.

Cistanche peut s'améliorerfonction rénale
Extrait de : « La déplétion à long terme des lymphocytes B est associée à la régénération de la fonction rénale » parSusanne V. Fleig, et al
---Dis. Immun Inflamm. 2021;9:1479–1488.
RÉFÉRENCES
1. Sato Y, Mii A, Hamazaki Y, et al. Les fibroblastes hétérogènes sous-tendent les tissus lymphoïdes tertiaires dépendant de l'âge dans leun rein. Aperçu JCI. 2016;1:87680.
2. Ruddle NH. Vaisseaux lymphatiques et organes lymphoïdes tertiaires. J Clin Invest. 2014;124:953‐959.
3. Legler DF, Loetscher M, Roos RS, Clark‐Lewis I, Baggiolini M, Moser B. La chimiokine 1 attirant les cellules B, une chimiokine CXC humaine exprimée dans les tissus lymphoïdes, attire sélectivement les lymphocytes B via BLR1/CXCR5. J Exp Méd. 1998;187:655‐660.
4. Dubey LK, Karempudi P, Luther SA, Ludewig B, Harris NL. Les interactions entre les cellules réticulaires fibroblastiques et les cellules B favorisent la lymphangiogenèse ganglionnaire mésentérique. Nat Commun. 2017;8:367.
5. Krautler NJ, Kana V, Kranich J, et al. Les cellules dendritiques folliculaires émergent de précurseurs périvasculaires omniprésents. Cellule. 2012 ; 150:194‐206.
6. Kratz A, Campos‐Neto A, Hanson MS, Ruddle NH. L'inflammation chronique causée par la lymphotoxine est une néogenèse lymphoïde. J Exp Méd. 1996;183:1461‐1472.
7. Lee Y, Chin RK, Christiansen P, et al. Recrutement et activation des lymphocytes T naïfs dans les îlots par la structure lymphoïde tertiaire dépendante des récepteurs de la lymphotoxine. Immunité. 2006;25:499‐509.
8. Cellules Segerer S. B et organes lymphoïdes tertiaires dans l'inflammation rénale.Un reinInt. 2008;73:5‐7.
9. Seleznik G, Seeger H, Bauer J, et al. Le récepteur de la lymphotoxine est une cible thérapeutique potentielle dans l'inflammation rénale.Un reinInt. 2016;89:113‐126.
10. Cohen CD, Calvaresi N, Armelloni S, et al. Infiltrats CD20 positifs dans la glomérulonéphrite membraneuse humaine. J Néphrol. 2005;18:328‐333.
11. Brix SR, Noriega M, Herden EM, et al. Organisation des infiltrats lymphocytaires dans la glomérulonéphrite associée aux ANCA. Histopathologie. 2018;72:1093‐1101.
12. Pei G, Zeng R, Han M, et al. Infiltration interstitielle rénale et néogenèse des organes lymphoïdes tertiaires dans la néphropathie à IgA. CJASN. 2014;9:255‐264.
13. Steines L, Poth H, Herrmann M, Schuster A, Banas B, Bergler T. Le facteur d'activation des cellules B (BAFF) est nécessaire au développement des organes lymphoïdes tertiaires intra-rénaux lors d'une transplantation rénale expérimentale chez le rat. IJMS. 2020;21:8045.
14. Steinmetz OM, Lange‐Hüsken F, Turner J‐E, et al. Le rituximab élimine les amas de lymphocytes B intrarénaux chez les patients présentant un rejet d'allogreffe vasculaire rénale. Transplantation. 2007;84:842‐850.
15. Kreimann K, Jang M‐S, Rong S, et al. Une lésion d'ischémie-reperfusion déclenche la libération de CXCL13 et le recrutement de lymphocytes B après allogéniqueun reintransplantation. Immunol avant. 2020;11:1204.
16. Cippà PE, Liu J, Sun B, et al. Une action tardive des lymphocytes B dans la réparation tissulaire dysfonctionnelleun reinblessure et transplantation. Nat Commun. 2019;10:1157.
17. Sato Y, Boor P, Fukuma S, et al. Les stades de développement du tissu lymphoïde tertiaire reflètent une blessure et une inflammation locales dans les reins de souris et d'humains. Rein Int. 2020;98:448‐463.
18. Floege J, Barbour SJ, Cattran DC et al, participants à la conférence. Prise en charge et traitement des maladies glomérulaires(partie 1) : conclusions d'unun reinmaladie: améliorer les résultats mondiaux (KDIGO) Controversies Conference. Kidney Int.2019;95:268‐280.
19. Trivin‐Avillach C, Beck LH. Prise en charge de la néphropathie membraneuse après MENTOR. Clin J Am Soc Nephrol. 2020;15:415‐417.
20. Rojas‐Rivera JE, Carriazo S, Ortiz A. Traitement de la néphropathie membraneuse idiopathique chez l'adulte : KDIGO cyclophosphamide et cyclosporine A sont sortis, le rituximab est la nouvelle norme. Clin Kidney J. 2019;12(5):629‐638.
21. Fervenza FC, Appel GB, Barbour SJ, et al. Rituximab ou cyclosporine dans le traitement de la néphropathie membraneuse. N Engl J Méd. 2019;381:36‐46.
22. Dahan K, Debiec H, Plaisier E, et al. Rituximab pour la néphropathie membraneuse sévère : un essai de 6 mois avec un suivi prolongé. JASN. 2017;28:348‐358.
23. Thaunat O, Patey N, Gautreau C, et al. Survie des lymphocytes B dans les organes lymphoïdes tertiaires intragreffe après traitement par le rituximab. Transplantation. 2008;85:1648‐1653.
24. Chang A, Henderson SG, Brandt D, et al. Réponses immunitaires médiées par les lymphocytes B in situ et inflammation tubulo-interstitielle dans la néphrite lupique humaine. J Immunol 2011;186:1849‐1860.
25. Inker LA, Schmid CH, Tighiouart H, et al, CKG‐EPI Investigators. Estimation du taux de filtration glomérulaire à partir de la créatinine sérique et de la cystatine C. N Engl J Med. 2012;367:20‐29.
26. Grayson PC, Eddy S, Taroni JN, et al. Voies métaboliques et immunométabolisme chez de raresun reinmaladies. Ann Rheum Dis.2018;77(8):1226‐1233.
27. Bankhead P, Loughrey MB, Fernández JA, et al. QuPath : logiciel opensource pour l'analyse d'images de pathologie numérique. Sci Rep.2017;7:16878.
28. Ruggenenti P, Cravedi P, Chianca A, et al. Rituximab dans la néphropathie membraneuse idiopathique. JASN. 2012;23:1416‐1425.
29. Fervenza FC, Abraham RS, Erickson SB, et al, Mayo NephrologyCollaborative Group. Thérapie par le rituximab dans la néphropathie membraneuse idiopathique : une étude de 2 ans. CJASN. 2010;5:2188‐2198.
30. Wang X, Cui Z, Zhang Y‐M, et al. Rituximab pour la néphropathie membraneuse idiopathique non réactive dans une cohorte chinoise. Greffe de cadran néphrol. 2018;33(9):1558‐1563.
31. Waldman M, Beck LH, Braun M, Wilkins K, Balow JE, Austin HA. Néphropathie membraneuse : une étude pilote d'un nouveau régime combinant la cyclosporine et le rituximab. Kidney Int Rep. 2016;1:73‐84.
32. Fernández‐Juárez G, Rojas‐Rivera J, van de Logt A‐E, et al. L'essai STARMEN indique qu'un traitement alterné avec des corticostéroïdes et du cyclophosphamide est supérieur au traitement séquentiel avec du tacrolimus et du rituximab dans la néphropathie membraneuse primaire. Rein Int. 2021;99:986‐998.
33. Crickx E, Weill J‐C, Reynaud C‐A, Mahévas M. Anti‐CD20‐mediated B‐cell depletion in autoimmun disease: successes, failures and futures perspectives. Rein Int. 2020;97:885‐893.
34. Fiorentino M, Tondolo F, Bruno F, et al. Traitement par rituximab dans la néphropathie membraneuse idiopathique. Clin Kidney J. 2016;9:788‐793.
35. Bagchi S, Subbiah AK, Bhowmik D, et al. Traitement par rituximab à faible dose dans la néphropathie membraneuse idiopathique résistante : une expérience monocentrique. Clin Kidney J. 2018;11:337‐341.
36. Keri KC, Blumenthal S, Kulkarni V, Beck L, Chongkrairatanakul T. Néphropathie membraneuse primaire : revue complète et perspective historique.Postgrad Med J. 2019;95(1119):23‐31.
37. Kim Y, Yoon HE, Chung BH, et al. Résultats cliniques et effets du traitement chez les patients âgés atteints de néphropathie membraneuse idiopathique. Coréen J Intern Med. 2019;34:1091‐1099.
38. Ruggenenti P, Debiec H, Ruggiero B, et al. Le titre d'anticorps anti-récepteur a2 de la phospholipase prédit le résultat post‐rituximab de la néphropathie membraneuse. J Am Soc Nephrol. 2015;26:2545‐2558.
39. Moroni G, Depetri F, Del Vecchio L, et al. Le rituximab à faible dose est peu efficace chez les patients atteints de néphropathie membraneuse primaire. Greffe de cadran néphrol. 2016 :gfw251.
40. Naesens M, Kuypers DRJ, Sarwal M. Néphrotoxicité des inhibiteurs de la calcineurine. Clin J Am Soc Nephrol. 2009;4:481‐508.
41. Kopp JB, Klotman PE. Mécanismes cellulaires et moléculaires de la néphrotoxicité de la cyclosporine. J Am Soc Nephrol. 1990;1:162‐179.
42. Docherty M‐H, O′Sullivan ED, Bonventre JV, Ferenbach DA.Sénescence cellulaire dans le rein. JASN. 2019;30:726‐736.
43. Glassock RJ, Règle AD. Vieillissement et reins : anatomie, physiologie et conséquences pour définir la chroniqueun reinmaladie. Néphron. 2016;134(1):25‐29.
44. Schmitt R, Melk A. Mécanismes moléculaires du vieillissement rénal. Rein Int. 2017;92:569‐579.
45. Sis B, Tasanarong A, Khoshjou F, Dadras F, Solez K, Halloran PF. Expression accélérée de l'inhibiteur du cycle cellulaire associé à la sénescence p16INK4A dans les reins atteints d'une maladie glomérulaire. Rein Int. 2007;71:218‐226.
46. Ruggenenti P, Ruggiero B, Cravedi P, et al. Rituximab dans le syndrome néphrotique idiopathique dépendant des stéroïdes ou fréquemment récurrent. JASN. 2014;25:850‐863.
