Maladie à changement minimal secondaire à la maladie du greffon contre l'hôte après une greffe allogénique de cellules hématopoïétiques pour le syndrome myélodysplasique
Jul 06, 2023
Abstrait
La maladie chronique du greffon contre l'hôte (cGVHD) est l'une des principales causes de mortalité sans rechute chez les receveurs d'une greffe allogénique de cellules hématopoïétiques (HCT). Alors que la norme de soins actuelle est proactive dans la détection de la GVHDc dans les poumons, le foie et la peau, la GVHDc impliquant les reins est une cause sous-reconnue et probablement sous-diagnostiquée de dysfonctionnement rénal post-HCT. Le syndrome néphrotique (SN) est une complication très rare du HCT qui est supposée être une manifestation glomérulaire de la cGVHD. Nous rapportons ici 2 cas de maladie à changement minime post-HCT probablement secondaire à la cGVHD. Dans les deux cas, l'apparition du SN a coïncidé avec la diminution progressive des inhibiteurs de la calcineurine, et 1 patient avait déjà reçu un diagnostic de cGVHD pulmonaire. Un patient a été traité par corticoïdes seuls et l'autre par corticoïdes et tacrolimus. Une rémission complète et prolongée a été obtenue dans les deux cas. Nos cas illustrent les implications de l'association entre cGVHD et post-HCT NS pour la prise en charge des patients, y compris l'importance d'obtenir une biopsie rénale pour établir un diagnostic histopathologique précis et guider le traitement approprié.
Mots clés
Syndrome néphrotique · Maladie du changement minimal · Maladie du greffon contre l'hôte · Biopsie rénale · Greffe allogénique de cellules hématopoïétiques.

Cliquez ici pour acheter le supplément Cistanche
Introduction
Bien que les progrès des greffes de cellules hématopoïétiques (HCT) aient considérablement amélioré les résultats pour les patients atteints du syndrome myélodysplasique (MDS) et de la leucémie aiguë, la HCT comporte toujours un risque substantiel de complications post-transplantation graves, notamment la rechute, l'infection opportuniste et la maladie du greffon contre l'hôte (GVHD). ). Alors que la norme de soins actuelle est proactive dans la reconnaissance des manifestations les plus courantes de la GVHD dans les poumons, la peau et le foie, les présentations atypiques impliquant d'autres systèmes d'organes posent un plus grand défi diagnostique. Un exemple est la GVHD du rein, une manifestation extrêmement rare et mal comprise de la GVHD. En raison de la rareté des cas signalés, la gamme complète des manifestations cliniques potentielles reste à voir et il n'y a pas de norme de soins établie. Cependant, il existe des preuves indiquant que la GVHD chronique (cGVHD) peut être une cause sous-diagnostiquée de dysfonctionnement rénal post-HCT.
La liste des causes potentielles de dysfonctionnement rénal chez les receveurs de HCT est longue et comprend l'hypovolémie, la septicémie, le syndrome de lyse tumorale, la néphrotoxicité induite par les médicaments et la GVHD. Une cause particulièrement rare mais potentiellement mortelle de dysfonctionnement rénal chez les receveurs de HCT est le syndrome néphrotique (NS). Parmi les patients atteints de SN post-HCT, la néphropathie membraneuse (MN) et la maladie à changement minimal (MCD) sont de loin les sous-types histopathologiques les plus couramment identifiés ; cependant, des rapports de cas de glomérulonéphrite membranoproliférative, de néphrite lupique de classe III, de glomérulosclérose segmentaire focale et de néphropathie à IgA ont également été publiés [1–4]. Un nombre croissant de preuves suggère que de nombreux cas de NS post-HCT peuvent représenter une manifestation glomérulaire de la cGVHD. Cette affirmation est étayée par l'observation que plus de 87 % des cas de SN post-HCT surviennent chez des patients atteints de GVHDc, ainsi que par la relation temporelle bien décrite entre la diminution des médicaments immunosuppresseurs et l'apparition du SN [5, 6]. D'autres preuves ont été découvertes grâce à des recherches scientifiques fondamentales sur des modèles murins de cGVHD montrant des modifications membranaires, des lésions mésangiales directes et des dépôts de complexes immuns [7–9].
Le mécanisme par lequel la cGVHD conduit au développement du SN post-HCT est mal compris, et la gamme complète des manifestations cliniques potentielles reste à voir. En raison de la rareté des cas signalés, il n'y a pas de norme de soins établie pour les bénéficiaires du HCT qui présentent des signes et des symptômes de SN. Ici, nous présentons 2 cas de MCD post-HCT probablement secondaire à la cGVHD du rein.

Cistanche tubulosa
Rapport de cas/Présentation de cas
Cas 1
Un homme de 64- ans ayant des antécédents de maladie des grands lymphocytes granuleux à cellules T et de goutte a été référé à la clinique pour une leucopénie chronique et des nodules annulaires récurrents de granulome sur le tronc, les bras et le visage. La biopsie de la moelle osseuse a révélé une légère dysplasie érythroïde et mégacaryocytaire avec un pourcentage de blastes légèrement élevé (5 %) évoquant un SMD avec un score IPSS-R à risque intermédiaire de 3,5. Le patient a terminé trois cycles d'azacitidine sans effets indésirables majeurs, et il a ensuite subi une HCT allogénique d'intensité réduite d'une donneuse appariée, non apparentée, avec une incompatibilité ABO mineure (donneur O plus vers receveur A plus). Il a reçu une prophylaxie GVDH post-transplantation standard avec du tacrolimus et du méthotrexate.
Soixante-treize jours après la greffe, le patient s'est présenté avec une histoire de 1-semaines de faiblesse généralisée, de fatigue, de dyspnée, de douleurs abdominales non focales et d'arthralgies non spécifiques, principalement au niveau des genoux et des chevilles. Peu de temps après, il a connu un début aigu d'altération de l'état mental et d'aphasie, provoquant une TDM et une IRM du cerveau, qui n'ont montré aucun signe de pathologie intracrânienne aiguë. En raison d'une préoccupation pour l'encéphalite, le patient a été traité empiriquement avec du céfépime, de l'azithromycine, de l'acyclovir et de l'ampicilline. Trois jours plus tard, il a développé une insuffisance respiratoire hypoxique aiguë qui, compte tenu de son état immunodéprimé, a fait craindre une pneumonie atypique ; cependant, les panels de pathogènes infectieux étaient négatifs. Finalement, une biopsie pulmonaire a révélé une lésion alvéolaire diffuse consistant en un syndrome pulmonaire idiopathique compatible avec la cGVHD. Il a été traité avec de l'étanercept et des stéroïdes à forte dose et maintenu sous tacrolimus jusqu'au jour 211 post-transplantation.
244 jours après la greffe, le patient s'est présenté au service des urgences avec une histoire de 1- semaines de dyspnée, de frissons, d'anorexie, de toux, d'étourdissements et de fatigue. Les analyses sanguines initiales étaient marquées par une anémie profonde (hémoglobine 4,1 g/dL), un nombre de réticulocytes de 10 %, une bilirubine sérique totale de 3,3 g/dL et une élévation de la créatinine sérique de 2,0 mg/ dL, avec sphérocytose sur frottis sanguin périphérique. Des études d'autoagglutination et d'antiglobuline ont été réalisées en raison d'un risque d'hémolyse, et les résultats étaient compatibles avec le syndrome des agglutinines froides. Le patient a bien répondu au traitement par corticoïdes, IgIV et transfusion de 2 culots globulaires, et le jour de sa sortie, son hémoglobine était stable à 7,0 g/dL. Après sa sortie, il a terminé une réduction progressive de la prednisone par voie orale et a reçu un total de quatre doses de rituximab.
280 jours après la greffe, le patient s'est de nouveau présenté aux urgences avec une hypertension, de la fatigue et un œdème périphérique initialement attribués à sa corticothérapie, mais a rapidement évolué vers un SN franc avec anasarque, urine mousseuse, aggravation de l'hypertension et {{1} gain de poids de } lb. Des études sériques ont révélé une créatinine de 3,3 mg/dL, une urée sanguine de 86 mg/dL et une albumine sérique de 2,2 g/dL. Les études d'urine ont montré une protéinurie massive avec un rapport protéines urinaires sur créatinine de 26,13 g/g, des cylindres hyalins modérés et une gravité spécifique de 1,017. L'échographie rénale a montré un épaississement diffus de la paroi vésicale, une échogénicité accrue sans hydronéphrose et une prostate légèrement hypertrophiée. Une biopsie rénale a été réalisée (Fig. 1) et la microscopie électronique a révélé un effacement sévère des processus du pied des podocytes sans anomalie pathologique dans les tubules proximaux et les capillaires péritubulaires. La microscopie optique a montré des glomérules d'apparence normale et aucun signe de dépôt de complexe immun sur la coloration par immunofluorescence, conduisant à un diagnostic de MCD.

Le patient a été traité par diurèse et prednisone orale 1 mg/kg et a repris le tacrolimus avec une nette amélioration de son œdème. La prednisone a été diminuée rapidement sur 3 mois, selon la préférence du patient, et le tacrolimus a été poursuivi pendant un total de 9 mois. Dans les 3 mois suivant le début du traitement, le rapport protéines urinaires/créatinine était tombé à<1 g/g. Kidney function continued to improve over the subsequent 6 months, reaching a new serum creatinine baseline of 1.6–1.9 mg/dL (estimated glomerular filtration rate 36–44 mL/ min/1.73 m2), consistent with chronic kidney disease stage III. Since the last office visit on day 680 posttransplant, the patient has experienced no further complications.

Pilules de cistanche
Cas 2
Une femme de 65- ans ayant des antécédents d'hypertension et de palpitations cardiaques a été référée à la clinique pour l'évaluation d'un éventuel SMD découvert lors d'une biopsie de la moelle osseuse réalisée dans le cadre d'un bilan d'anémie. Un examen de la biopsie a révélé une augmentation du pourcentage de blastes (12 %) compatible avec le sous-type de SMD EB-2 avec un score IPSS-R de risque intermédiaire de 4. Le patient a toléré 6 cycles d'azacitidine sans effets secondaires majeurs et a ensuite subi HCT allogénique de conditionnement à intensité réduite provenant d'un donneur apparié, non apparenté et compatible ABO (RA-/D plus A plus ). Elle a reçu une prophylaxie post-transplantation standard de la GVHD avec de la cyclosporine et du méthotrexate. Son parcours hospitalier a été compliqué par une fibrillation auriculaire nouvellement diagnostiquée qui s'est résolue avec le métoprolol, et elle a été libérée sous prophylaxie appropriée. La réduction progressive de la cyclosporine a commencé au jour 135 post-transplantation.
268 jours après la greffe, le patient s'est présenté à l'hôpital avec une oligurie et une anasarque. Au moment de son admission, sa cyclosporine avait été réduite à 25 mg tous les deux jours et elle était sous prophylaxie avec TMP-SMX 160 mg 3 fois par semaine. Le laboratoire à l'admission était remarquable pour une créatinine sérique élevée (6,0 mg/dL à partir d'une ligne de base de 1,0 mg/dL) et une protéinurie massive (rapport protéine/créatinine dans l'urine spot 13,65 g/g). Une biopsie rénale a été réalisée (Fig. 2) et la microscopie électronique a montré un effacement sévère des processus du pied des podocytes avec des glomérules d'apparence normale à la microscopie optique et aucun dépôt de complément ou d'immunoglobuline à l'immunofluorescence, compatible avec la MCD.
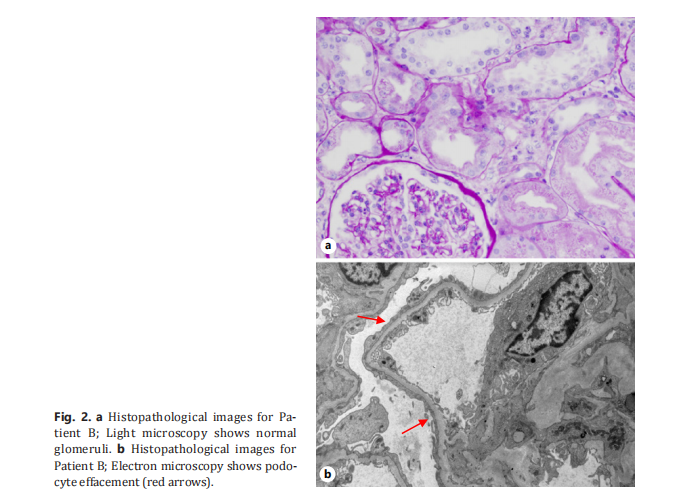
Le patient a subi une hémodialyse (HD) via un cathéter HD temporaire et a commencé le tacrolimus 0.5 mg deux fois par jour et la méthylprednisolone 1 g/kg/jour. La méthylprednisolone a été poursuivie pendant 11 jours et le tacrolimus a été interrompu après 7 jours en raison d'un risque d'altération de la récupération rénale dans un contexte aigu en raison d'une vasoconstriction induite par le médicament. Un cathéter de dialyse tunnelisé a été placé en prévision des besoins HD à long terme. Elle a finalement été renvoyée chez elle sous prednisone 60 mg par jour, avec pour objectif de subir une HD 3 fois par semaine. Dans la semaine suivant la sortie, la diurèse et la clairance du soluté du patient s'étaient nettement améliorées et la dialyse a été interrompue après un total de 6 séances. Une réduction complète de la prednisone a été réalisée 4 mois après la sortie, avec résolution de sa protéinurie néphrotique. Environ 570 jours après la greffe, elle n'a pas eu besoin d'une HD supplémentaire et sa créatinine sérique est actuellement stable à 1,1 mg/dL.

Herba Cistanche
Discussion
La relation entre la cGVHD et le SN a des implications importantes pour la prise en charge du SN post-HCT. Le pilier actuel du traitement de la MCD est la monothérapie aux glucocorticoïdes, qui entraîne une rémission complète dans 80 à 95 % des cas de MCD chez l'adulte [10]. En revanche, la MCD post-HCT est souvent résistante aux glucocorticoïdes, avec un taux de réponse d'environ 22 % [9]. Les autres patients nécessitent un traitement combiné avec des inhibiteurs de la calcineurine, le mycophénolate mofétil ou le rituximab [11–15]. De même, le MN post-HCT a tendance à être résistant aux glucocorticoïdes, avec des taux de réponse comparables à ceux observés dans le MGN idiopathique, environ 11 % [9]. Alors que les schémas thérapeutiques pour la MCD et la MN chez les receveurs de HCT sont similaires, il existe des différences significatives dans le pronostic de ces 2 entités. Dans une revue systématique de 116 patients traités pour un SN post-HCT, les patients atteints de MCD se sont rétablis en une médiane de 1,75 mois, tandis que le temps médian de récupération pour les patients atteints de MN était de 7 mois. Les résultats globaux du traitement différaient également, avec une rémission complète obtenue chez 81,3 % des patients atteints de MCD et 59,1 % des patients atteints de MN [9].
Compte tenu de ces différences de traitement et de pronostic, la biopsie rénale est essentielle à la prise en charge des receveurs de HCT qui présentent une protéinurie néphrotique. Cependant, les receveurs de HCT sont souvent médicalement complexes et la biopsie rénale peut être sous-performante dans cette population en raison d'un risque élevé de complications telles que des saignements ou des infections. La biopsie rénale doit être envisagée chez tous les patients chez qui il existe un risque de SN post-HCT et doit idéalement être réalisée avant de commencer un traitement immunosuppresseur dans la mesure du possible. Chez les patients présentant une contre-indication claire à la biopsie, un essai empirique de corticoïdes doit être envisagé. Cependant, étant donné la forte probabilité de maladie résistante aux corticostéroïdes, les cliniciens doivent maintenir un seuil bas pour commencer des agents immunosuppresseurs supplémentaires. Beyar-Katz et al. [9] ont proposé un traitement empirique par corticoïdes, une surveillance étroite et une réévaluation de la protéinurie à 12–16 semaines pour déterminer la nécessité d'immunosuppresseurs supplémentaires, bien qu'il n'y ait pas eu d'études examinant l'efficacité de cette approche. De plus, malgré le rôle de l'immunosuppression à long terme dans le rejet d'organe solide du rein, il n'y a pas suffisamment d'informations dans la littérature détaillant la prophylaxie la plus optimale pour la GVHD du rein ou les méthodes efficaces pour le traitement à long terme de la cGVHD du rein.

Gélules Cistanche
Ici, nous avons décrit 2 cas de MCD post-HCT favorisés pour être causés par la cGVHD du rein. Dans les deux cas, l'apparition du SN a coïncidé avec la diminution progressive des inhibiteurs de la calcineurine, faisant suspecter une GVHD comme cause sous-jacente. La biopsie a été obtenue peu de temps après l'apparition des symptômes, permettant un diagnostic rapide de MCD. Les deux patients ont commencé à prendre des corticostéroïdes et du tacrolimus, bien que le tacrolimus ait été arrêté après une semaine chez le patient 2, et les deux patients ont eu une excellente réponse avec une rémission prolongée après le traitement. Ces cas mettent en évidence l'importance du lien entre la cGVHD et le SN, et ses implications pour les soins aux patients. Les cliniciens doivent être conscients que la cGVHD est présente chez la plupart des patients atteints de SN post-HCT, dont la grande majorité nécessitera une immunosuppression supplémentaire au-delà de la monothérapie aux glucocorticoïdes. De plus, la biopsie rénale ne doit pas être retardée sauf si nécessaire, car elle est essentielle pour garantir un diagnostic précis, un traitement approprié et un résultat plus favorable.
Les références
1 Fraile P, Pilar F, Vazquez L, Lourdes V, Caballero D, Dolores C, et al. Maladie chronique du greffon contre l'hôte du rein chez les patients ayant subi une greffe allogénique de cellules souches hématopoïétiques. Eur J Haematol. août 2013;91(2):129–34.
2 Kim JY, Lee MY, Kim B, Park CW, Chang YS, Chung S. Glomérulonéphrite membranoproliférative suite à une allogreffe de cellules souches hématopoïétiques. Clin Exp Néphrol. 2010 décembre;14(6):630–2.
3 Hu SL, Colvin GA, Rifai A, SuzukiH, Novak J, Esparza A, et al. Glomérulonéphrite après greffe de cellules hématopoïétiques : néphropathie à IgA avec excrétion accrue d'IgA1 déficient en galactose. Greffe de cadran néphrol. 2010 mai;25(5):1708–13.
4 Hingorani S. Complications rénales de la transplantation de cellules hématopoïétiques. N Engl J Méd. 9 juin 2016;374(23): 2256–67.
5 Brukamp K, Doyle AM, Bloom RD, Bunin N, Tomaszewski JE, Cizman B. Syndrome néphrotique après transplantation de cellules hématopoïétiques : les lésions glomérulaires représentent-elles une maladie rénale du greffon contre l'hôte ? Clin J Am Soc Nephrol. juillet 2006;1(4):685–94.
6 Srinivasan R, Balow JE, Sabnis S, Lundqvist A, Igarashi T, Takahashi Y, et al. Syndrome néphrotique : une complication à médiation immunitaire sous-reconnue de la greffe de cellules hématopoïétiques allogéniques non myéloablatives. Br J Haematol. octobre 2005;131(1):74–9.
7 Padhi P, Muchayi T, Teske E, Kuperman M, Barrantes F. Maladie à changement minimal après greffe de cellules souches hématopoïétiques : une manifestation de la maladie chronique du greffon contre l'hôte. J Onco-Néphrol. 1er février 2020;4(1–2):37–40.
8 Chu YW, Gress RE. Modèles murins de maladie chronique du greffon contre l'hôte : aperçus et problèmes non résolus. Greffe de Moelle Sanguine Biol. avril 2008;14(4):365–78.
9 Beyar-Katz O, Davila EK, Zuckerman T, Fineman R, Haddad N, Okasha D, et al. Syndrome néphrotique de l'adulte après greffe de cellules souches hématopoïétiques : la pathologie rénale est le meilleur prédicteur de la réponse au traitement. Greffe de Moelle Sanguine Biol. 2016 juin;22(6):975–81.
10 Colattur SN, Korbet SM. Résultat à long terme de la maladie à changement minime idiopathique de l'adulte. Saudi J Kidney Dis Transpl. 2000 septembre;11(3):334–44.
11 Mak SK, CD court, Mallick NP. Résultat à long terme de la néphropathie à changement minimal de l'adulte. Greffe de cadran néphrol. 1996 novembre;11(11):2192–201.
12 Black DA, Rose G, Brewer DB. Essai contrôlé de prednisone chez des patients adultes atteints du syndrome néphrotique. Br Med J. 1970 22 août;3(5720):421–6.
13 Nolasco F, Cameron JS, Heywood EF, Hicks J, Ogg C, Williams DG. Syndrome néphrotique à changement minimal de l'adulte : un suivi à long terme. Rein Int. 1986 juin;29(6):1215–23.
14 Rao PS. Syndrome néphrotique chez les patients ayant subi une greffe de cellules souches du sang périphérique. Suis J Kidney Dis. 2005 avril ; 45(4):780–5.
15 Dhakal B, Singavi A, Cohen EP, Dangal M, Palmer J, Dall A, et al. GVHD chronique et syndrome néphrotique d'apparition concomitante chez les receveurs d'une allogreffe. Incidence, modèle et résultats thérapeutiques. Greffe de moelle osseuse. 2015 mars;50(3):449–51.
Omar Elghawy 1, John S. Wang 1, Alexander C. Hafey 1, Amand 1, D. Renaghan 2 Rachel M. Whitehair 3, Tamila L. Kindwall-Keller 4,
1 École de médecine, Université de Virginie, Charlottesville, VA, États-Unis ;
2 Division de néphrologie, Université de Virginie, Charlottesville, VA, États-Unis ;
3 Département de pathologie, Université de Virginie, Charlottesville, VA, États-Unis ;
4 Division d'hématologie et d'oncologie, Université de Virginie, Charlottesville, VA, États-Unis






