Partie Ⅰ : maladie rénale et risque de démence : une étude de cohorte nationale danoise
Apr 10, 2023
Abstrait
Objectifs
Il est actuellement difficile de savoir si la maladie rénale est un facteur de risque de démence. Nous avons étudié la relation entre la maladie rénale et le risque de démence future.
Conception et réglage
Étude de cohorte du registre historique national danois, basée sur des données du 1er janvier 1995 au 31 décembre 2016.
Intervenants
Tous les patients diagnostiqués avec une maladie rénale et une cohorte de la population générale appariée sans maladie rénale (l'âge, le sexe et l'année du diagnostic de maladie rénale appariés 1:5).
Mesures de résultats primaires et secondaires
Démence toutes causes confondues et ses sous-types : maladie d'Alzheimer, démence vasculaire et autres démences spécifiques ou non précisées. Nous avons utilisé l'analyse de régression de Cox pour calculer l'incidence cumulée (risque) et les rapports de risque (HR) de 5- année pour les résultats.
Résultats
La cohorte de l'étude comprenait 82 690 patients atteints de maladie rénale et 413 405 personnes de la population générale. Les taux de mortalité de 5- et 10- ans étaient deux fois plus élevés chez les patients atteints de maladie rénale que dans la population générale. Le risque de démence toutes causes confondues sur 5-ans était de 2,90 % (intervalle de confiance à 95 % : 2,78 % à 3,08 %) chez les patients atteints d'insuffisance rénale et de 2,98 % (2,92 % à 3,04 %) dans la population générale. Par rapport à la population générale, les RR corrigés pour la démence toutes causes confondues chez les patients atteints d'insuffisance rénale étaient de 1,06 (1,00 à 1,12) au cours de l'5-année de suivi et de 1,08 (1,03 à 1,12) au cours toute la période d'études. Les estimations du risque pour les sous-types de démence variaient considérablement, avec des estimations plus faibles pour la maladie d'Alzheimer et des estimations plus élevées pour la démence vasculaire.
conclusion
Les patients diagnostiqués avec une maladie rénale ont une incidence légèrement accrue de démence, principalement causée par une démence vasculaire. De plus, les patients atteints de maladie rénale peuvent ne pas recevoir de diagnostic de démence en raison d'une mortalité élevée et d'autres comorbidités prioritaires.
Mots clés
Maladie du rein; démence;Suppléments de Cistanche.

Cliquez ici pour acheterExtrait de cistanchepour garder votre rein en bonne santé
Introduction
La démence est un trouble neurologique lié à l'âge courant et progressif diagnostiqué lorsque la déficience cognitive acquise est suffisamment grave pour altérer le fonctionnement social et/ou professionnel Bien que l'incidence de la démence ait légèrement diminué au cours des 30 dernières années, la prévalence de la démence est en augmentation dans le monde , probablement en raison de l'augmentation de l'espérance de vie Cela impose des coûts importants aux personnes et aux familles touchées, ainsi qu'aux soins de santé et à la société.
Les maladies rénales sont une autre maladie dont la prévalence est élevée (près de 10 %) et croissante, en partie en raison du vieillissement de la population et de l'incidence croissante de l'hypertension et du diabète.
Les maladies rénales et la démence partagent des facteurs de risque communs tels que le vieillissement, l'hypertension, le diabète, l'hyperlipidémie et la physiopathologie de la maladie des petits vaisseaux. Un lien potentiel entre les maladies rénales et la démence peut être la susceptibilité commune des tissus rénaux et cérébraux aux lésions vasculaires. Les maladies rénales sont associées au stress oxydatif, à l'inflammation chronique et à une coagulation altérée, et peuvent également affecter le cerveau ou le système vasculaire cérébral indirectement ou directement par le métabolisme. troubles et toxines urémiques.
Une précédente étude basée sur la population à Taïwan a trouvé un rapport de risque (HR) de 1,41 pour la démence toutes causes confondues chez les patients diagnostiqués avec une maladie rénale (N=37049) par rapport à la population générale (N=74098. Cependant , ces résultats peuvent ne pas s'appliquer aux populations européennes et l'étude taïwanaise n'a pas examiné les différences potentielles entre les sous-types de démence. En outre, dans des études antérieures définissant l'insuffisance rénale comme une protéinurie persistante ou un débit de filtration glomérulaire estimé (DFGe) inférieur à 60 mL/min/1,73 m2 , différents résultats ont été rapportés. Par conséquent, il n'est pas certain que la néphropathie soit associée au risque de démence. Nous avons étudié la démence toutes causes confondues et les sous-types de démence (maladie d'Alzheimer, démence vasculaire et autres démences) dans une étude de cohorte nationale.
Méthodes
Nous avons suivi les Lignes directrices pour l'amélioration de la notification des études épidémiologiques observationnelles sur les études de cohorte épidémiologique.

Cistanche aux herbes
Cohorte d'étude
Au cours de la période d'étude allant du 1er janvier 1995 au 31 décembre 2016, nous avons mené une étude de cohorte à l'échelle nationale incluant tous les patients danois diagnostiqués à l'hôpital avec une maladie rénale et une cohorte de comparaison de la population générale appariée sans maladie rénale.
L'organigramme de la cohorte de l'étude est illustré à la figure 1. Au cours de la période d'étude, nous avons identifié 122 670 patients avec un premier diagnostic de maladie rénale. Ensuite, nous avons exclu les patients décédés (N=32196) ou qui ne vivaient pas au Danemark (N=465) dans l'année suivant le diagnostic d'insuffisance rénale. D'autres critères d'exclusion étaient un diagnostic de démence (N=1909) et des symptômes prodromiques de démence, c'est-à-dire une déficience cognitive légère et un syndrome amnésique (N=303) avant le diagnostic de maladie rénale. De plus, nous avons exclu les patients diagnostiqués avec une démence (N=1300) et des symptômes prodromiques de démence (N=156) dans l'année suivant le diagnostic de maladie rénale, car un diagnostic de démence pendant cette période est peu probable être la conséquence d'une maladie rénale. Enfin, nous avons limité la cohorte aux patients adultes âgés de 18 ans et plus. Les 82 690 patients restants constituaient notre cohorte d'insuffisance rénale. Pour chaque patient de la cohorte d'insuffisance rénale, 5 personnes de la population générale sans diagnostic d'insuffisance rénale avant la date d'index ont été sélectionnées au hasard et appariées sur la base de l'âge (année de naissance), du sexe et de l'année civile de la date d'index (c'est-à-dire la date du diagnostic de maladie rénale). L'appariement a été effectué en tant qu'appariement individuel pour remplacer la cohorte de comparaison de la population générale composée de 413 405 patients qui ne souffraient pas de démence, de troubles cognitifs légers, de syndrome amnésique ou de maladie rénale avant l'entrée dans l'étude.
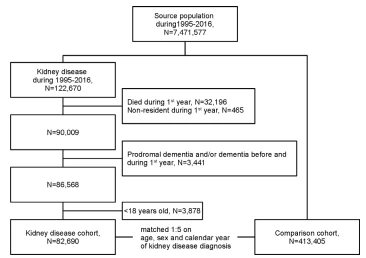
Figure 1 : Organigramme de l'étude. les individus de la cohorte de patients qui ont développé une maladie rénale pendant 1995-2016 et la cohorte de comparaison de la population générale appariée.
Diagnostics
Les diagnostics de néphropathie (exposition), de démence (résultat), de troubles cognitifs légers, de syndrome amnésique et de covariables étaient basés sur les diagnostics obtenus à partir du registre national danois des patients et/ou du registre central danois de recherche en psychiatrie. Ces registres couvraient tous les hôpitaux du Danemark et enregistraient les admissions hospitalières depuis 1977 et 1969, respectivement, et les visites de spécialistes ambulatoires depuis 1995. Nous avons utilisé tous les diagnostics primaires et secondaires de sortie pour toutes les visites hospitalières et ambulatoires, mais avons exclu les visites aux urgences (car les diagnostics dans de tels cas peut être provisoire et donc moins valide). Les diagnostics ont été déterminés selon la classification internationale des maladies de l'Organisation mondiale de la santé, révision 8 (ICD-8), jusqu'à la fin de 1993, suivie de la révision 10 (ICD-10). Nous avons retenu la date d'hospitalisation ou de début de suivi ambulatoire comme date de tous les diagnostics.
Maladie du rein
Dans l'analyse principale, nous avons utilisé une définition élargie de la maladie rénale qui comprenait la maladie rénale chronique ainsi que plusieurs autres maladies rénales persistantes, le traitement par dialyse et la transplantation rénale. Fait important, cette définition élargie de la maladie rénale n'incluait pas les lésions rénales aiguës et/ou potentiellement réversibles. Dans les analyses de sensibilité, nous n'avons utilisé que les maladies rénales chroniques (limitées à la CIM-8 792 et la CIM-10 N18) comme exposition pour la démence toutes causes confondues. Le pronostic global d'amélioration de la maladie rénale (KDIGO) définit le rein chronique comme un DFGe persistant (3 mois) de 60 mL/min/1,73 m2 ou une insuffisance rénale, généralement déterminée par la présence d'une protéinurie.
Démence
La validité de la démence toutes causes confondues était élevée, avec une valeur prédictive positive de 86 % des sous-types de démence enregistrés au Danemark s'excluant mutuellement, et nous n'avons utilisé que le premier sous-type de démence codé : maladie d'Alzheimer, démence vasculaire et autres démence (spécifiée ou non précisée), cette dernière constituant la majorité des diagnostics de démence. Étant donné qu'environ un tiers des autres cas de démence non précisés peuvent être attribuables à la maladie d'Alzheimer,19 nous avons également inclus le résultat combiné de la maladie d'Alzheimer et d'autres démences.
Covariables
Nous avons inclus les maladies cardiovasculaires (MCV), les facteurs de risque de MCV, (tout) cancer et le statut socio-économique comme facteurs de confusion potentiels en raison de leur association avec les maladies rénales et la démence. Toutes les covariables ont été évaluées avant l'entrée dans l'étude. les covariables cardiovasculaires étaient l'angine de poitrine, l'infarctus du myocarde, l'accident vasculaire cérébral, la maladie artérielle périphérique, la thromboembolie veineuse, l'insuffisance cardiaque, la valvulopathie et la fibrillation auriculaire. Les covariables associées aux facteurs de risque de MCV étaient l'hypercholestérolémie, l'hypertension, l'obésité, le diabète sucré et la bronchopneumopathie chronique obstructive (tabagisme). -médicaments hypertenseurs du registre national danois des prescriptions, qui contient des données individuelles détaillées sur toutes les prescriptions ambulatoires depuis 1995.
Les covariables associées au statut socioéconomique sont le niveau de scolarité le plus élevé, le revenu personnel total et le statut d'emploi, qui ont été obtenus à partir de la base de données exhaustive de la recherche sur le marché du travail créée en 1981. Le niveau de scolarité est classé comme faible (école primaire seulement), moyen (école secondaire et /ou diplôme professionnel collégial) et élevé (baccalauréat, maîtrise ou diplôme supérieur). Le revenu personnel total est classé par quartiles. Le statut d'emploi a été classé comme employé, retraité et chômeur. Nous avons utilisé le statut d'emploi 12-24 mois avant l'entrée dans l'étude, car le statut d'emploi au cours de l'année précédant le diagnostic de maladie rénale peut sous-estimer le statut d'emploi maximal.
Avantages Cistanche
analyses statistiques
Nous avons comparé l'incidence cumulée de décès (risque) et de démence toutes causes confondues (en tenant compte des risques concurrents de décès) dans les cohortes d'insuffisance rénale et de comparaison. Les RR pour la démence toutes causes confondues et les sous-types de démence et leurs IC à 95 % correspondants ont été calculés à l'aide de l'analyse de régression de Cox en utilisant la durée de l'étude comme échelle de temps. les hypothèses de risque proportionnel ont été testées graphiquement par des tracés log-log, et aucune violation n'a été détectée. Dans le modèle de Cox non ajusté, l'âge, le sexe et l'année civile de la date de l'indice ont été contrôlés, car il s'agissait des critères d'appariement. Cependant, pour tenir compte de la méthode d'appariement, les correspondances n'ont pas pu être entièrement conservées en raison d'un biais de sélection intégré, de sorte que le modèle de Cox ajusté incluait l'âge, le sexe et l'année civile de la date de l'index, ainsi que d'autres facteurs de confusion potentiels. Les participants avec des valeurs manquantes (1 % du revenu personnel total et 11 % du statut d'emploi et du niveau d'éducation) ont été exclus de l'analyse ajustée. 1 an à compter de la date de l'indice jusqu'au 31 décembre 2016, diagnostic de démence ou dépistage, immigration ou décès, selon la première éventualité. La période de suivi minimale était de 1 an et la période maximale était de 22 ans. Étant donné que tous les diagnostics et statuts de vie et d'immigration étaient enregistrés dans le Registre national, nous n'avons eu aucune perte de suivi. Nous avons effectué des analyses stratifiées prédéfinies pour l'âge (18-49, 50-59, 60-74, 75-84 et 85 ans), le sexe, l'année civile de la date d'index (1995-2003 ou 2004-2016), maladies cardiovasculaires, facteurs de risque de maladies cardiovasculaires, facteurs socio-économiques et durée du suivi (1-5, 1-10 et 1-22 ans).
Enfin, pour évaluer si le risque de démence toutes causes confondues était associé à la gravité de l'insuffisance rénale, nous avons stratifié la cohorte d'insuffisance rénale en fonction de la présence ou de l'absence d'insuffisance rénale. Toutes les analyses ont été effectuées à l'aide de SAS V.9.4 (SAS Institute).

Cistanche normalisé
LES RÉFÉRENCES
1. Arvanitakis Z, Shah RC, Bennett DA. Diagnostic et prise en charge de la démence : une revue. JAMA 2019;322:1589–99.
2. Knopman DS. L'énigme de la diminution de l'incidence de la démence. JAMA Netw Open 2020;3:e2011199.
3. Rapport mondial sur la maladie d'Alzheimer 2015 : l'impact mondial de la démence : une analyse de la prévalence, de l'incidence, des coûts et des tendances. tome 2020, 2015.
4. Collaboration GBD sur les maladies rénales chroniques. Fardeau mondial, régional et national de l'insuffisance rénale chronique, 1990-2017 : une analyse systématique de l'étude sur le fardeau mondial de la maladie 2017. Lancet 2020 ;395:709–33.
5. Barnes DE, Yaffe K. L'effet projeté de la réduction des facteurs de risque sur la prévalence de la maladie d'Alzheimer. Lancet Neurol 2011;10:819–28.
6. Ikram MA, Vernooij MW, Hofman A, et al. La fonction rénale est liée à la maladie des petits vaisseaux cérébraux. AVC 2008;39:55–61.
7. Bugnicourt JM, Godefroy O, Chillon JM, et al. Troubles cognitifs et démence dans l'IRC : l'axe rein-cerveau négligé. J Am Soc Nephrol 2013;24:353–63.
8. Cheng KC, Chen YL, Lai SW, et al. Les patients atteints de maladie rénale chronique courent un risque élevé de démence : une étude de cohorte basée sur la population à Taïwan. BMC Néphrol 2012;13:129.
9. Deckers K, Camerino I, van Boxtel MPJ, et al. Risque de démence dans l'insuffisance rénale : une revue systématique et une méta-analyse d'études prospectives. Neurologie 2017 ; 88 : 198–208.
10. Gabin JM, Romundstad S, Saltvedt I, et al. Augmentation modérée de l'albuminurie, de la maladie rénale chronique et de la démence incidente : l'étude HUNT. BMC Néphrol 2019;20:261.
11. Takae K, Hata J, Ohara T, et al. L'albuminurie augmente les risques de maladie d'Alzheimer et de démence vasculaire chez les personnes âgées japonaises vivant dans la communauté : l'étude Hisayama. J Am Heart Assoc 2018;7.
12. Paterson EN, Williams MA, Passmore P, et al. Le taux de filtration glomérulaire estimé n'est pas associé à la maladie d'Alzheimer dans une cohorte d'Irlande du Nord. J Alzheimers Dis 2017;60:1379–85.
13. Berger I, Wu S, Masson P, et al. Cognition dans l'insuffisance rénale chronique : une revue systématique et une méta-analyse. BMC Med 2016;14:206.
14. Heide-Jørgensen U, Adelborg K, Kahlert J, et al. Stratégies d'échantillonnage pour sélectionner les cohortes de comparaison de la population générale. Clin Epidemiol 2018;10:1325–37.
15. Mors O, Perto GP, Mortensen PB. Le registre central de recherche psychiatrique danois. Scand J Public Health 2011;39:54–7.
16. Schmidt M, Schmidt SAJ, Sandegaard JL, et al. Le registre national danois des patients : un examen du contenu, de la qualité des données et du potentiel de recherche. Clin Epidemiol 2015;7:449–90.
17. Schmidt M, Schmidt SAJ, Adelborg K, et al. Le système de santé danois et la recherche épidémiologique : des contacts de soins de santé aux enregistrements de la base de données. Clin Epidemiol 2019;11:563–91.
18. Levey AS, de Jong PE, Coresh J, et al. La définition, la classification et le pronostic de l'insuffisance rénale chronique: un rapport de conférence sur les controverses KDIGO. Kidney Int 2011;80:17–28.
19. Phung TKT, Andersen BB, Høgh P, et al. Validité des diagnostics de démence dans les registres hospitaliers danois. Dement Geriatr Cogn Disord 2007;24:220–8.
20. Webster AC, Nagler EV, Morton RL, et al. Maladie rénale chronique. Lancet 2017;389:1238–52.
21. Pottegård A, Schmidt SAJ, Wallach-Kildemoes H, et al. Profil des ressources de données : le registre national danois des ordonnances. Int J Epidemiol 2017;46:798–798f.
22. Petersson F, Baadsgaard M, Thygesen LC. Registres danois sur l'affiliation personnelle au marché du travail. Scand J Public Health 2011;39:95–8.
Alisa D Kjaergaard1,2. Benjamin R. Johannesen2. Henrik T Sørensen2,3. Victor W Henderson2,4. Christian F. Christiansen2
1. Steno Diabetes Center Aarhus, Hôpital universitaire d'Aarhus, Aarhus, Danemark
2. Département d'épidémiologie clinique, Hôpital universitaire d'Aarhus, Aarhus, Danemark
3. Excellence Research Center, Université de Stanford, Stanford, Californie, États-Unis
4. Départements d'épidémiologie et de santé des populations et de neurologie et sciences neurologiques, Université de Stanford, Stanford, Californie, États-Unis
