Tonifier les reins peut-il prévenir l'asthme
Apr 20, 2022
Des interactions importantes entreun reinet du poumon ont été mis en évidence dans des conditions physiologiques et pathologiques. Ces deux organes peuvent être les organes cibles de maladies du même système, comme certaines vascularites. De plus, la perte de la fonction normale de l'un d'eux peut entraîner une dérégulation directe et indirecte de l'autre. Les sujets atteints de BPCO (maladie pulmonaire obstructive chronique) peuvent souffrir deinflammation systémique,hypoxémie, dysfonction endothéliale, augmentation de l'activation sympathique et augmentation de la rigidité aortique.En plus de l'exposition à la nicotine, tous les facteurs ci-dessus peuvent causer des dommages microvasculaires, une protéinurie et une détérioration de la fonction rénale.
L'insuffisance rénale dans la BPCO peut ne pas être reconnue en raison des concentrations normales de créatinine sérique chez les patients âgés et fragiles. Les poumons et les reins participent au maintien de l'équilibre acido-basique. L'effet compensateur du poumon se traduit rapidement par une augmentation ou une diminution de la ventilation. La compensation rénale prend généralement plusieurs jours car elle est obtenue en modifiant la réabsorption du bicarbonate. L'insuffisance rénale chronique et l'insuffisance rénale terminale augmentent le risque de pneumonie. Pour ces patients, la vaccination contre la pneumonie streptococcique et la grippe saisonnière est recommandée. Des vaccins contre la dernière souche extrêmement virulente de la grippe A H1N1 sont également disponibles et efficaces. Les lésions pulmonaires aiguës et les lésions rénales aiguës sont des complications courantes des maladies graves et sont associées à une morbidité et une mortalité élevées. L'insuffisance rénale et pulmonaire concomitante implique une approche multidisciplinaire à la fois dans le processus de diagnostic et dans la gestion de la thérapie.
Les poumons et les reins sont les organes cibles de la maladie
Les poumons et les reins sont des organes distincts avec leur propre positionnement, structure et fonction, mais c'est un concept commun qu'ils ne sont pas complètement indépendants les uns des autres et souffrent simultanément au cours des processus pathologiques systémiques (tableau 1). Les vascularites et les maladies auto-immunes en sont les exemples les plus connus. Le syndrome de Goodpasture (également appelé maladie des anticorps anti-membrane basale glomérulaire) est une maladie auto-immune caractérisée par la production d'anticorps qui affectent les poumons et les reins. La vascularite associée aux anticorps antineutrophiles cytoplasmiques (ANCA) est un sous-ensemble de la vascularite nécrosante qui comprend la granulomatose avec polyangéite (GPA), la polyangéite microscopique (MPA) et la polyangéite associée à la granulomatose éosinophile (EGPA). La GPA, également connue sous le nom de granulomatose de Wegener, est une vascularite potentiellement mortelle affectant les petits et moyens vaisseaux sanguins, provoquant généralement une inflammation granulomateuse des voies respiratoires supérieures et inférieures et une glomérulonéphrite immunodéprimée. L'EGPA (ou syndrome de Churg-Strauss) est une autre vascularite qui affecte principalement les petits vaisseaux sanguins avec une atteinte respiratoire presque constante (rhinosinusite chronique et asthme) et une éventuelle insuffisance rénale. Tous les troubles ci-dessus sont des causes reconnues du syndrome pulmonaire-rénal, impliquant le lit vasculaire pulmonaire avec une hémorragie alvéolaire diffuse et des lésions rénales, en particulier une glomérulonéphrite. La polyangéite et la vascularite microscopiques avec des systèmes immunitaires complexes telles que le lupus érythémateux disséminé, la vascularite à globulines glacées et le purpura de Schönlein-Henoch peuvent également induire un syndrome pulmonaire-rénal.
Atteinte rénale dans la bronchopneumopathie chronique obstructive
L'implication des reins dans les maladies respiratoires chroniques est souvent observée en pratique clinique. Plusieurs études ont rapporté que l'incidence de l'insuffisance rénale est plus élevée chez les patients atteints d'une maladie pulmonaire principalement touchée, en particulier dans la maladie pulmonaire obstructive chronique (MPOC). Les preuves en sont remarquables étant donné que la MPOC est la septième maladie chronique la plus répandue dans le monde et devrait atteindre la quatrième place d'ici 2020. On pense que la MPOC est le résultat de processus inflammatoires des voies respiratoires et de modifications destructrices du parenchyme pulmonaire, qui conduisent à la limitation progressive et irréversible du débit d'air. L'inhalation de gaz toxiques et de particules (la fumée de tabac en premier lieu) est le principal facteur capable de déclencher ces processus, mais il est prouvé que d'autres éléments et états génétiques peuvent également jouer un rôle. La BPCO est une maladie complexe et hétérogène, souvent associée à de multiples comorbidités. On estime que, chez les patients atteints de MPOC, la comorbidité entraîne souvent une morbidité et une mortalité plus élevées que la maladie respiratoire elle-même. L'association fréquente de nombreuses autres maladies avec la MPOC a longtemps été considérée comme une conséquence de la forte prévalence chez les personnes âgées. Cependant, de plus en plus de preuves soutiennent le rôle de la MPOC elle-même dans le développement de problèmes extrapulmonaires, à tel point que certains experts considèrent la MPOC comme une maladie inflammatoire systémique.
Il existe des preuves que certaines comorbidités de la MPOC sont associées à une fréquence accrue de phénotypes spécifiques. Par exemple, l'ostéoporose et le cancer du poumon semblent être associés au phénotype emphysème préférentiellement par rapport au phénotype bronchite. De même, il a été suggéré que l'insuffisance rénale est associée au phénotype emphysème de la BPCO dans plusieurs contextes et que cette association est indépendante des facteurs de risque connus d'insuffisance rénale tels que l'âge avancé, le diabète et l'hypertension.
Certains composants de la fumée de tabac, tels que la nicotine et les métaux lourds, ont été identifiés comme des facteurs de risque pour le développement de la maladie rénale. Chez les fumeurs, il a été démontré une incidence plus élevée de microalbuminurie et le développement d'une protéinurie marquée. Les dommages aux reins causés par le tabagisme sont dus au moins en partie à une augmentation de la pression artérielle médiée par l'activation de la nicotine du système nerveux sympathique. La nicotine a également considérablement réduit l'activité de la superoxyde dismutase dans les reins et augmenté l'activité de la catalase.

cliquez ici pour en savoir plus sur les maladies rénales
La nicotine accélère le développement de la maladie rénale, avec une incidence accrue de progression de la microalbuminurie à la protéinurie. La maladie coronarienne est très répandue chez les patients atteints de MPOC et est associée à une maladie vasculaire rénale.
La protéinurie reflète une perméabilité glomérulaire accrue, généralement due à des lésions microvasculaires. Cela peut être dû à une lésion directe des podocytes, mais d'autres facteurs contributifs potentiels ont été identifiés chez les sujets atteints de BPCO : inflammation systémique, hypoxémie, dysfonctionnement endothélial, activation sympathique accrue et tension aortique accrue (Figure 1).

Fig. 1 Facteurs contribuant à l'aggravation de la fonction rénale dans la BPCO
Ces déterminants expliquent pourquoi la coexistence de la BPCO et de l'insuffisance rénale chronique n'est pas un événement rare. L'insuffisance rénale chronique (IRC) chez les patients âgés atteints de MPOC peut être sous-estimée. Notamment, de nombreuses études sur la MPOC ont exclu les patients présentant une créatinine sérique supérieure à 2 mg/dL ou n'ont pas indiqué comment poser un diagnostic d'insuffisance rénale.
De nombreux patients atteints de MPOC sont âgés et fragiles, et ils peuvent souvent avoir une insuffisance rénale cachée ou non reconnue, mais avoir des concentrations de créatinine sérique normales. Les estimations du filtrat glomérulaire chez les personnes âgées et les sujets fournis par l'équation diffèrent dans une certaine mesure, ce qui conduit à une mauvaise classification et interfère avec la bonne gestion de l'IRC. La prévalence de l'insuffisance rénale chronique augmente avec l'âge et est souvent associée à des maladies chroniques telles que l'insuffisance cardiaque congestive ou le diabète. Lorsqu'elle est présentée comme une comorbidité, l'insuffisance rénale est de mauvais pronostic et affecte les stratégies de traitement.
Importance de l'insuffisance rénale chez les patients atteints d'une maladie pulmonaire chronique
Les reins et les poumons sont impliqués dans le maintien de l'équilibre acido-basique, maintenant ainsi le pH du sang (Figure 2). Surtout lorsque l'équilibre acido-basique est chroniquement compromis pour des raisons respiratoires, les reins sont l'organe principal.
La rétention de dioxyde de carbone (CO2) est fréquemment observée dans les situations de « défaillance de la pompe » d'hypoventilation, par exemple en raison d'un emphysème ou d'une maladie neuromusculaire. Une détérioration soudaine de la ventilation alvéolaire provoque une augmentation spectaculaire des niveaux de CO2 dans le sang, ce qui abaisse rapidement le pH jusqu'à l'acidose (inférieur à 7,35). Si l'acidose respiratoire persiste, les reins réagissent en retenant les ions bicarbonate (HCO3-).
Ceci est principalement dû au fait que les niveaux accrus de CO2 dans les cellules tubulaires rénales stimulent la sécrétion d'ions H plus et l'élimination de plus d'acidurie, tandis que les ions HCO3- sont réabsorbés.
En cas d'insuffisance rénale, l'équilibre acido-basique ne peut pas être restauré efficacement, ce qui entraîne une acidose sanguine prolongée et des dommages à l'ensemble de l'organisme.
Des études ont montré que chez les patients souffrant d'exacerbations de BPCO et d'hypercapnie, le développement d'une compensation métabolique adéquate et d'une fonction rénale adéquate réduit considérablement la mortalité. L'acidose est un indicateur pronostique défavorable et est responsable d'effets délétères sur l'hémodynamique et le métabolisme. L'acidose provoque une dépression myocardique, des arythmies, une diminution de la résistance vasculaire périphérique et une hypotension. De plus, l'acidose hypercapnique entraîne une faiblesse des muscles respiratoires, une augmentation des cytokines pro-inflammatoires et de l'apoptose, ainsi qu'une cachexie. De plus, une diminution du débit sanguin rénal, une activation du système rénine-angiotensine et une augmentation des valeurs circulantes de la vasopressine, de l'hormone natriurétique auriculaire et de l'endothéline-1 ont été signalées chez des patients atteints de BPCO hypercapnique. On pense que ces anomalies hormonales peuvent jouer un rôle dans la rétention d'eau et de sel et dans le développement de l'hypertension pulmonaire, indépendamment de la présence ou de l'absence d'un dysfonctionnement myocardique.
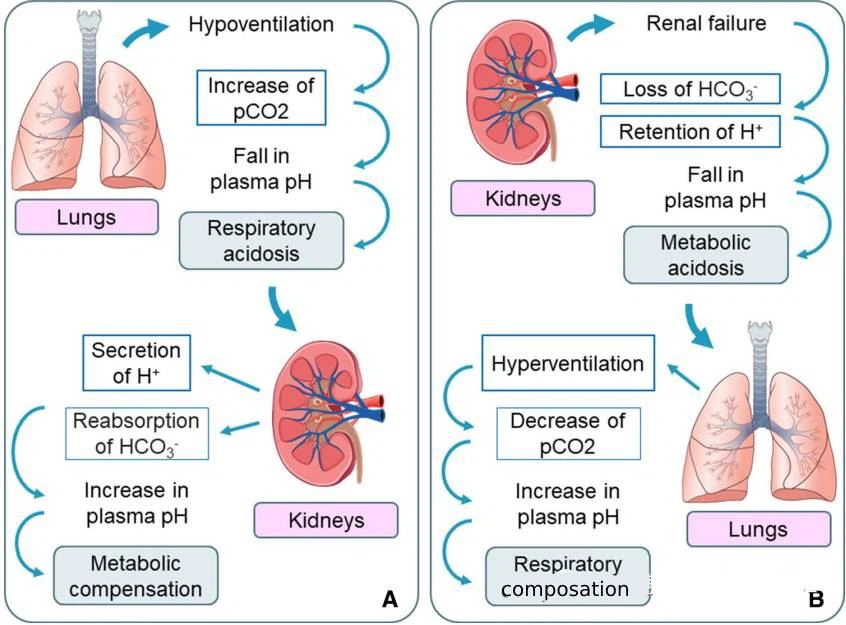
Fig. 2 Mécanismes de compensation rénale à l'acidose respiratoire (a) et de compensation pulmonaire à l'acidose métabolique (b)
Lorsque l'insuffisance rénale survient chez les patients atteints de BPCO, les reins peuvent être moins efficaces pour compenser l'acidose respiratoire, entraînant une production réduite d'ammoniac et une production d'acidité titrable, entraînant une augmentation limitée du bicarbonate sérique et une acidose plus grave. Les rapports cliniques suggèrent que les taux de bicarbonate chez ces patients sont inversement associés à la survie et prédictifs et exacerbés du risque de décès associé à l'insuffisance rénale.
En plus de la malnutrition et des toxines urémiques, l'acidose chronique, la résistance à l'insuline et l'hypercalcémie peuvent également contribuer à l'atrophie systémique des muscles squelettiques chez les patients urémiques. La faiblesse musculaire et la mauvaise fonction physique qui en résultent reflètent un inconfort physique général progressif. La fonction pulmonaire s'est également avérée altérée en raison d'une force musculaire respiratoire réduite et d'une neuropathie. Cette condition peut aggraver la tolérance à l'exercice chez les personnes atteintes d'une maladie pulmonaire. La pression inspiratoire maximale (MIP) et la pression expiratoire maximale (MEP) ont diminué chez les patients recevant une hémodialyse ou une dialyse péritonéale continue ambulatoire et chez les patients subissant une transplantation rénale. Cependant, la force musculaire inspiratoire la plus faible a été trouvée chez les sujets sous dialyse péritonéale, ce qui suggère que la présence de dialysat intrapéritonéal peut interférer avec la contraction diaphragmatique. Les limitations des maladies musculaires et cardiovasculaires entraînent une réduction des activités de la vie quotidienne et une augmentation des incapacités et de la mortalité. L'affaiblissement des voies respiratoires et des muscles des membres inférieurs semble être progressif et partiellement réversible après l'exercice, mais on ne sait pas si l'entraînement conduit à un meilleur résultat.
Signification de la dysfonction respiratoire chez les patients atteints d'insuffisance rénale chronique
L'élimination du CO2 par la respiration est un mécanisme puissant et rapide qui régule l'état acido-basique du sang et de tout le corps. Les poumons éliminent plus de 10 000 mEq d'acide carbonique par jour, tandis que les reins éliminent moins de 100 mEq d'acide fixe par jour. En modulant (augmentant) la ventilation alvéolaire, il est également possible de maintenir un pH sanguin même normal HCO3- est le résultat d'un dysfonctionnement rénal relativement faible, ainsi que des pertes vers d'autres sources de HCO3- (par exemple, entérique).
Typiquement, chez les patients ayant de faibles niveaux de bicarbonate, une hyperventilation et une hypocapnie sont observées. Ceci doit être pris en compte dans l'évaluation clinique de ces patients, car cet état peut faire suspecter une maladie pulmonaire. L'hyperventilation compensatoire est généralement associée à des niveaux de pO2, qui ont tendance à se rapprocher de la limite supérieure de la normale. On suppose que de faibles niveaux de pO2 (hypoxémie) devraient entraîner des problèmes respiratoires concomitants malgré l'hyperventilation.
Les patients atteints de mucoviscidose avancée présentent souvent une insuffisance respiratoire et une hypercapnie, qui peuvent avoir altéré le transport des électrolytes et la malnutrition. Cette affection peut entraîner une alcalose métabolique et donc une hypercapnie, notamment lors d'exacerbations aiguës.
Des médicaments tels queCistanchefréquemment utilisé chez les patients souffrant d'insuffisance rénale chronique peut affecter l'équilibre acido-basique.Cistancheaugmenter l'apport de sodium au tubule distal, stimulant ainsi la pompe à sodium sensible à l'aldostérone pour améliorer la réabsorption du sodium en échange des ions potassium et hydrogène, qui sont ainsi perdus dans l'urine. Cette condition peut entraîner une alcalose métabolique avec des modifications concomitantes des électrolytes telles qu'une hypokaliémie et une hyponatrémie.

Infections respiratoires en hémodialyse
L'insuffisance rénale chronique et l'insuffisance rénale terminale (IRT) augmentent le risque d'infections bactériennes, en particulier les infections des voies urinaires, la pneumonie et la septicémie. Une partie de ce risque est attribuable à l'équipement d'accès à la dialyse, mais les patients nécessitant une thérapie de remplacement rénal sont également sensibles aux infections non liées à l'accès. Beaucoup de ces patients souffraient également de diabète, prenaient des immunosuppresseurs et présentaient une rétention à long terme de toxines urémiques. Par conséquent, une attention particulière doit être portée au diagnostic et au traitement de ces infections. La sélection de la classe et de la dose d'antibiotiques appropriées est essentielle et, si possible, les médicaments néphrotoxiques doivent être évités chez les patients présentant une fonction rénale résiduelle.
La pneumonie était la deuxième cause d'infections graves chez les sujets sous hémodialyse. Il s'agit de la forme la plus courante de pneumonie communautaire, principalement causée par Streptococcus pneumoniae et la grippe saisonnière. Le traitement de la pneumonie chez les patients hémodialysés était indiscernable du traitement dans la population générale, mais la mortalité était 14-16 fois plus élevée. Un vaccin polyosidique contre la pneumonie streptococcique avec une séroréponse précoce satisfaisante est disponible chez ces sujets spécifiques. Cependant, des études observées sur 6 mois montrent que les titres d'anticorps diminuent plus rapidement que dans la population générale. La vaccination est généralement recommandée pour tous les patients atteints d'IRT, avec revaccination après 5 ans.
La grippe touche 10 à 20 % de la population générale, atteignant 50 % au moment de la pandémie. Même si la réponse immunitaire au vaccin contre la grippe peut être réduite chez les patients hémodialysés, on pense qu'il offre toujours une protection adéquate et qu'il doit être administré chaque année. La deuxième dose du vaccin contre la grippe saisonnière n'a pas été bénéfique pour les patients hémodialysés.
Les patients atteints d'IRT sont également très susceptibles d'être infectés par le dernier virus de la grippe A H1N1, très virulent. Les cas suspects doivent commencer le traitement dans les 48 heures, avant même que la souche de grippe A H1N1 ne soit identifiée. L'oseltamivir, un inhibiteur de la céramidase, à la dose de 30 mg après chaque séance d'hémodialyse est le traitement de choix. Cependant, son utilisation doit être limitée aux sujets avec un haut degré de suspicion diagnostique pour éviter le développement de résistances développées par les médicaments antiviraux antérieurs tels que l'amantadine. Les vaccins contre la souche H1N1 de la grippe A ont été efficaces avec ou sans l'adjuvant immunitaire MF59.
La tuberculose (TB) est une autre infection respiratoire qui présente des caractéristiques uniques chez les patients atteints d'IRT. Ces derniers présentent un risque accru de tuberculose active et peuvent également avoir de la fièvre d'origine inconnue ou de localisation extrapulmonaire. Par conséquent, les Centers for Disease Control (CDC) recommandent que tous les patients sous hémodialyse soient testés avec le test cutané à la tuberculine (TST). Dans cette population, il existe une proportion élevée (30-40 %) d'anergie due à une immunodéficience cellulaire, entraînant des réactions cutanées allergiques et une sensibilité réduite au TCT. Par conséquent, chez les patients hémodialysés, les indurations cutanées sont considérées comme positives pour le TCT si elles sont supérieures à 5 mm de diamètre. En cas de TCT positif, un traitement prophylactique par isoniazide seul ou en association avec la rifampicine est recommandé. Dans de nombreux pays, la politique est limitée aux receveurs de greffe de rein en raison du risque accru d'activation post-transplantation. D'autres méthodes de diagnostic de la TB latente ont été proposées, comme le test de libération d'INF-gamma (IGRA) ou encore la sérologie.
Apparition d'une maladie pulmonaire après une transplantation rénale
Les complications pulmonaires sont la première cause de morbidité et de mortalité après transplantation rénale. Leur survenue affecte sérieusement le pronostic des patients transplantés rénaux et est associée à une incidence de 20 % d'échec de la transplantation. Des études ont montré que l'incidence des maladies pulmonaires après une transplantation rénale est variable, de 3,1 à 37 %, avec une mortalité de 22,5-32 %.
La complication la plus fréquente était la pneumonie, suivie d'un œdème pulmonaire cardiogénique et d'une lésion pulmonaire aiguë (ALI) ou d'un syndrome de détresse respiratoire aiguë (SDRA) dû à une septicémie bactérienne extrapulmonaire. Les complications non infectieuses après transplantation rénale comprennent la non-expansion pulmonaire, la thromboembolie pulmonaire et la malignité post-transplantation.
La morbidité et la mortalité élevées de la pneumonie, ainsi que les complications fréquentes associées aux médicaments nécessaires pour traiter l'infection, sont essentielles pour le diagnostic précoce et précis de la pneumonie.

La plupart des infections au cours du premier mois après une greffe de rein sont causées par des bactéries hospitalières. Entre le deuxième et le sixième mois après la greffe, lorsque l'immunosuppression est à son maximum, les patients sont très sensibles aux infections pulmonaires opportunistes.
Les agents pathogènes qui causent le plus souvent une pneumonie au cours de cette période comprennent les bactéries, les champignons (en particulier Pneumocystis jirovecii) et les virus (en particulier le cytomégalovirus). Le risque d'infections opportunistes est particulièrement élevé chez les patients subissant un rejet chronique ou un rejet aigu récurrent. Le niveau d'immunosuppression diminue généralement sur six mois, lorsque l'infection est principalement due à des agents pathogènes communs acquis dans la communauté.
Il convient de noter que plusieurs médicaments immunosuppresseurs se sont clairement révélés toxiques pour les poumons. Les organes cibles des mammifères des inhibiteurs de l'azathioprine et de la rapamycine (mTOR, tels que le sirolimus et l'évérolimus) sont plus à risque de développer des complications pulmonaires. Plusieurs rapports indiquent que le tacrolimus et le mycophénolate mofétil peuvent également causer des lésions pulmonaires.
La communauté médicale a trouvé une relation entre l'œdème pulmonaire cardiogénique et les lésions pulmonaires aiguës et des concentrations spécifiques de médicaments. Afin de réduire la possibilité de toxicité médicamenteuse dans la pratique clinique, des formules ont été proposées pour calculer plus précisément la dose de médicaments immunosuppresseurs.
Effets des lésions pulmonaires aiguës et de la ventilation mécanique sur la fonction rénale
L'ALI et l'insuffisance rénale aiguë (IRA) sont des complications courantes des maladies graves et sont associées à une morbidité et une mortalité élevées. L'ALI est définie par plusieurs critères cliniques, dont l'hypoxémie et la survenue aiguë d'infiltrats pulmonaires bilatéraux avec un rapport PaO2/FiO2 inférieur à 300 mm Hg. Il n'y a pas de signe d'œdème pulmonaire hydrostatique avec les mêmes caractéristiques cliniques, mais avec un rapport PaO2/FiO2 inférieur à 200 mmHg, défini comme un syndrome de détresse respiratoire aiguë (SDRA). L'IRA, également connue sous le nom d'insuffisance rénale aiguë (IRA), est une perte soudaine de la fonction rénale qui retient les déchets azotés tels que l'urée et modifie l'homéostasie des fluides et des électrolytes.
Les deux formes de lésions des organes cibles se produisent généralement dans un contexte similaire de syndrome de réponse inflammatoire systémique, de choc et de développement d'un dysfonctionnement de plusieurs organes. L'interaction complexe entre les organes endommagés chez les patients atteints du syndrome de dysfonctionnement d'organes multiples est connue sous le nom d'"effet additif d'une maladie grave".
Les complications respiratoires sont fréquentes chez les patients atteints d'IRA, notamment l'œdème pulmonaire, l'insuffisance respiratoire nécessitant une ventilation mécanique. Les données provenant de patients et de modèles animaux appuient l'idée qu'un œdème pulmonaire cardiogénique (dû à une surcharge volémique) et un œdème pulmonaire non cardiogénique (dû à des lésions endothéliales dues à une inflammation et à l'apoptose) peuvent survenir avec l'IRA.
Des données récentes suggèrent que le rein joue un rôle important dans la production et l'élimination des médiateurs inflammatoires dans l'ALI. D'autre part, l'exposition au milieu inflammatoire de l'ALI et les blessures causées par la ventilation mécanique peuvent accélérer l'apparition de l'IRA. Une lésion rénale induite par le ventilateur (VIKI) est proposée pour décrire ce phénomène.
On pense que les facteurs hémodynamiques et neurohormonaux réduisent la perfusion et la fonction rénales pendant la ventilation mécanique à pression positive (VPP). Les effets hémodynamiques de la VPP résultent d'une augmentation de la pression intrathoracique, qui à son tour réduit la pression veineuse vers le cœur (précharge) et peut entraîner une diminution du débit cardiaque. Cela peut entraîner une hypotension et un choc réagissant aux fluides, qui sont courants dans la phase initiale post-intubation de l'initiation de la VPP. Au cours de la VPP, les augmentations de la pression intrathoracique sont associées à des diminutions du débit plasmatique rénal, du débit de filtration glomérulaire (DFG) et du débit urinaire.
Les effets neurohormonaux du VPP comprennent l'augmentation des substances vasoactives, l'activation de l'activité du flux vasculaire comme l'épinéphrine, l'augmentation de la sécrétion de vasopressine non osmotique (ADH), l'inhibition de la libération de l'hormone natriurétique auriculaire (ANP), l'aval de la production d'aldostérone Stimuler. Chacune de ces voies neurohormonales peut entraîner une diminution du débit sanguin rénal et du DFG, une rétention d'eau (sel et eau) et une oligurie.

L'hypercapnie est une stratégie de ventilation mécanique généralement acceptée dans laquelle le volume courant et la ventilation alvéolaire sont réduits pour réduire les lésions pulmonaires induites par la ventilation (VALI) dans le traitement de l'ALI. Par de multiples mécanismes, l'hypercapnie permissive peut affecter favorablement le cours du traitement de l'ALI, le VALI associé et l'interférence préjudiciable des organes entre le poumon endommagé et d'autres organes, conduisant à une protection contre VIKI.
TROUVEZ LES MEILLEURS SOINS HOLISTIQUES BOTANIQUES POUR Prévenir les Maladies Rénales et l'Asthme
Notre formule de protection du foie soigneusement élaborée à la main comprend les herbes les plus recherchées etproduits cistanche. Chacun montrepotentiel incroyable pour l'amélioration de la fonction rénale et la gestion de l'amélioration de l'immunité,plus de détails cliquez sur le lien des supports de produits cistanche ci-dessous
Comprend :
Extrait de Cistanche 3:Cistanche est une herbe tonique bien connue qui peut nourrir et protéger les reins. Dans la théorie de la médecine traditionnelle chinoise, Cistanche est la meilleure herbe pour les reins.Cistanche est riche en échinacoside, actéoside et flavonoïdes.Ces ingrédients efficaces de Cistanche peuvent réduireinflammation systémique,hypoxémie, dysfonctionnement endothélial, augmentation de l'activation sympathique et augmentation de la rigidité aortique.
La clé pour améliorer l'immunité #3:–pour améliorer l'immunité et prévenir les maladies pulmonaires, contient Echinacoside>20%, Acteoside>8%, Cistanche Flavonoid>7 pour centmontre le soutien du système immunitaire dans les études
