Détection de la réponse immunitaire humorale et cellulaire au vaccin anti-SRAS-CoV-2 BNT162b2 chez les femmes qui allaitent et les personnes naïves et précédemment infectées
Nov 20, 2023
Cette étude a exploré les réponses humorales et cellulaires au vaccin à ARNm anti-SARS-CoV-2 BNT162b2 chez les femmes allaitantes et les individus naïfs et séropositifs au cours des six premiers mois suivant la vaccination. Soixante et un volontaires vaccinés avec deux doses du vaccin à ARNm BNT162b2 ont été inscrits à l’étude. Un test ELISA développé en interne a été utilisé pour la quantification des anticorps spécifiques du SRAS-CoV-2 RBD. L'expression des marqueurs de surface cellulaire et l'analyse de l'IFN intracellulaire ont été réalisées par cytométrie en flux. Les concentrations d'IFN-, d'IL-6 et de TNF ont été déterminées par ELISA. Une augmentation significative des taux d’anticorps IgG anti-RBD a été observée 14 jours après la première dose de vaccin (p< 0.0001) in serum and milk. The expression of CD28 on CD4+ T cells was significantly higher compared to baseline (p< 0.05). There was a significant increase (p≤ 0.05) in the B cell lymphocyte subset after revaccination and an increased percentage of CD80+ B cells. The expression of IFN-γ in peripheral blood lymphocytes, CD3+ T cells, and serum was significantly increased (p< 0.05). No significant difference in immune response was observed between breastfeeding women and other study participants. The anti-SARS CoV-2 BNT162b2 mRNA vaccine induced measurable and durable immune response in breastfeeding women and naïve and previously infected individuals.

Avantages du cistanche pour les hommes : renforcer le système immunitaire
Cliquez ici pour voir les produits Cistanche Enhance Immunity
【Demandez plus】 E-mail :cindy.xue@wecistanche.com / Whats App : 0086 18599088692 / Wechat : 18599088692
1. Introduction
La propagation mondiale du virus SRAS-CoV-2 après l'enregistrement du premier cas particulier le 31 décembre 2019 à Wuhan, en Chine, a conduit à une pandémie mondiale de maladie à coronavirus-19 (COVID{{ 5}}), avec environ 648 millions de cas et 6,6 millions de décès jusqu'au 18 décembre 20221. La mortalité liée au COVID-19 a été associée à une production excessive de cytokines proinflammatoires telles que l'IL-6, le TNF- et IL-1, ce qu'on appelle la « tempête de cytokines », qui peut entraîner un syndrome de détresse respiratoire aiguë et des lésions tissulaires importantes entraînant une défaillance multiviscérale2. Cependant, les améliorations rapides en matière de diagnostic, de traitement et d’introduction de la vaccination devraient contribuer à une baisse constante du nombre de personnes infectées, des besoins d’hospitalisation et, à terme, à une réduction du taux de mortalité. En Serbie, le premier cas officiellement enregistré s'est produit le 6 mars 2020 et la vaccination a débuté le 24 décembre 2020. Actuellement, quatre vaccins sont disponibles pour la population générale : Vero Cell-Inactivated (Sinopharm), Vaxzevria (ChAdOx{{ 22}}S [recombinant], AstraZeneca), Spoutnik V (Gam-COVID-Vac, Gamaleya) et Comirnaty (BNT162b2, BioNTech-Pfizer). Outre la production d’anticorps spécifiques, la réponse immunitaire efficace contre le SRAS-CoV-2 nécessite l’activation de l’immunité cellulaire. Les composants de l'immunité cellulaire, y compris les lymphocytes T CD auxiliaires4+ et CD cytotoxiques8+, les cellules tueuses naturelles (NK) et les lymphocytes B, dans les premières heures et jours suivant l'exposition à ce virus, devraient réduire les symptômes de la maladie, empêchant ainsi la progression de la maladie, l’hospitalisation et la mort. Les lymphocytes T auxiliaires (T) activés peuvent tuer indirectement les cellules infectées et soutenir la fonction des lymphocytes B et la réponse en anticorps en produisant de l'interféron (IFN-) 3,4. Il a été démontré que le phénotype T1 est associé à une moindre gravité de la maladie COVID-195, donc les stratégies de développement de vaccins COVID-19 devraient également prendre en compte la possibilité d'activation des cellules T pour la production d'IFN. L'immunité cellulaire contre le SRAS-CoV-2 serait détectable jusqu'à 6 mois après l'infection chez plus de 90 % des individus6. Ainsi, on s’attendait à ce que la vaccination donne naissance à une immunité cellulaire mesurable qui contribuerait à la lutte contre la pandémie. De nouveaux résultats ont montré qu'en plus d'activer les lymphocytes B dans les centres germinaux7, les vaccins à ARNm anti-SARS-CoV-2 devraient générer des réponses des lymphocytes T CD4+ et CD8+ spécifiques aux protéines de pointe8. Bien que le titre d’anticorps soit généralement corrélé à l’efficacité du vaccin, les lymphocytes B et T jouent un rôle important dans la protection lors d’une réexposition aux antigènes viraux. Ces cellules mémoire B et T devraient être générées par les vaccins à ARNm du SRAS-CoV-2 et devraient jouer un rôle dans le contrôle de la réplication du virus, limitant ainsi la dissémination virale9. Bien qu'aucun événement indésirable grave n'ait été signalé, la réponse spécifique à la vaccination anti-SRAS-CoV-2 chez les femmes enceintes et allaitantes et les nourrissons dont les mères ont reçu le vaccin pendant l'allaitement est toujours en cours d'évaluation et reste un sujet controversé10,11. Cette recherche visait à explorer pour la première fois les réponses humorales et cellulaires mensuelles au vaccin anti-SARS-CoV-2 ARNm BNT162b2 chez les femmes allaitantes et chez les individus naïfs et séropositifs, au cours des six premiers mois suivant la vaccination en Serbie, et un suivi autodéclaré de deux ans de la sécurité à long terme.
matériel et méthodes
Conception de l’étude, collecte et traitement des échantillons.
Au total, 61 volontaires (45 SRAS-CoV-2 naïfs, 16 SRAS-CoV-2 récupérés selon les rapports confirmés par PCR) ont été inscrits à l'étude et suivis entre janvier et novembre 2{ {11}}21. Le délai moyen entre l’infection naturelle et la vaccination chez les individus précédemment infectés était de 3,18 ± 0,98 mois, avec une fourchette de 2 à 5 mois. Tous les participants étaient âgés de plus de 18 ans et ne présentaient aucun signe d’infection respiratoire au moment de la vaccination. La plupart des participants étaient des professionnels de santé de l'Institut d'oncologie et de radiologie de Serbie (44 ; 72 %). Les participants ont été vaccinés avec deux doses du vaccin à ARNm BNT162b2 (à 3 semaines d’intervalle). Toutes les prises de sang ont été effectuées dans des centres médicaux agréés selon des protocoles et une observation stricts. Quatre participantes étaient des mères allaitantes qui se sont portées volontaires pour faire correspondre des échantillons de sang et de lait. Des échantillons ont été collectés à 6- points dans le temps : point 1 : pré-vaccination (référence), point 2 à 14 jours après la vaccination primaire, point 3 à 1 mois après la vaccination primaire, point 4 à 2 mois après la vaccination primaire, entre 5 et 3 mois après la vaccination primaire et entre 6 et 6 mois après la vaccination primaire. 10 à 20 ml de sang périphérique ont été prélevés à chaque instant, ainsi que 1 ml de lait pour 4 femmes allaitantes participantes. Le sérum a été obtenu à partir du sang périphérique par centrifugation immédiatement après le prélèvement sanguin et conservé à -20 degrés. Les cellules mononucléées du sang périphérique (PBMC) ont été isolées du sang hépariné en utilisant un gradient de densité Lymphoprep (Nypacon, Oslo, Norvège), centrifugées à 500 g pendant 40 min et lavées trois fois dans un milieu de culture (CM) RPMI 1640 (Sigma, St. Louis , MO) complété par 10 % de sérum de veau fœtal (FCS) (Sigma, St. Louis, MO). Après lavage, les PBMC ont été immédiatement utilisées pour l’analyse immunophénotypique. L'étude a été approuvée par le comité d'éthique de l'Institut d'oncologie et de radiologie de Serbie (n° 899-01 du 01.04.2021.) et tous les participants ont signé un consentement éclairé. Tous les participants ont été interrogés par du personnel médical expérimenté. Un suivi à long terme autodéclaré des effets indésirables post-vaccination a été réalisé pendant deux ans après la première dose de vaccin.

cistanche tubulosa-améliorer le système immunitaire
Détection et quantification des anticorps spécifiques du SRAS‑CoV‑2 RBD.
L'expression du RBD de la protéine de pointe du SRAS-CoV-2 (NCBI : YP_009724390, AA319-541) a été réalisée dans la lignée de cellules T HEK-293 à la suite d'une procédure publiée précédemment12. . La protéine recombinante a été purifiée jusqu'à homogénéité et le rendement obtenu était de 5{{20}}0 mg par L de culture cellulaire. En bref, la protéine RBD recombinante a été utilisée pour recouvrir des plaques de puits 96- à fond gras (Thermo Scientific NUNC-MaxiSorp, USA) à une concentration finale de 10 ug/mL (50 μL/puits) dans un tampon de revêtement (15 mM Na2CO3/35 mM NaHCO3, pH 9,5) à 4 degrés pendant la nuit. Les plaques ont été lavées avec du TBS contenant 0,05 % de Tween 20 (TBST) et bloquées avec 1 % de BSA dans du TBST pendant 2 h à 37 degrés. Les sérums dilués ont été incubés à 37 degrés pendant 1 h dans du TBST contenant 0,1 % de BSA, puis les plaques ont été lavées avec du TBST. Pour la détermination des IgG spécifiques totales, un anticorps conjugué de chèvre anti-IgG-humaine-AP (Novus Biologicals, USA) a été dilué au 1/1000 dans une solution de blocage et ajouté aux puits. Après 1 heure d'incubation à 37 degrés, les plaques ont été lavées 5 fois avec du TBST et développées avec du 4-phosphate de nitrophényle pendant 1 heure à 37 degrés. L'absorbance a été mesurée à 450 nm (A450).
Analyse cytométrique en flux.
L'immunophénotype de la surface cellulaire des cellules mononucléées du sang périphérique (PBMC) a été identifié à l'aide des combinaisons suivantes d'anticorps monoclonaux (mAb) directement marqués : CD3FITC/CD28PE/CD4PerCP, CD80PE/CD19PerCP, CD80PE/CD14PerCP (Becton Dickinson, San José, États-Unis). Les échantillons ont été préparés comme décrit précédemment13 en utilisant 1 × 105 PBMC fraîchement isolées dans 100 μL de RPMI 1640 additionné de 10 % de sérum de veau fœtal (FCS, Sigma), incubées pendant 30 min à 4 degrés avec 20 μL de combinaison appropriée d'AcM, lavées deux fois avec solution saline tamponnée au phosphate (PBS) glacée et fixée avec 1% de paraformaldéhyde avant les analyses FACS. L'expression des marqueurs de surface a été quantifiée sur le cytomètre en flux FACSCalibur (Becton – Dickinson, San Jose, USA). Un total de 10 000 à 50 000 événements contrôlés vérifiés en tant que lymphocytes du sang périphérique (PBL) et monocytes, en fonction de leurs caractéristiques physiques, de leurs caractéristiques de diffusion directe (FSC) et de leurs caractéristiques de diffusion latérale (SSC). ), ont été collectés par échantillon et analysés à l'aide du logiciel CellQUEST. Les sous-ensembles de cellules ont été exprimés en pourcentage dans le sang périphérique.
Analyse IFN intracellulaire.
Pour la coloration intracellulaire de l'IFN 1 ×, 106 PBMC ont été incubées avec du Phorbol 12-myristate 13-acétate (PMA) (50 ng/mL) plus de l'ionomycine (500 ng/mL) pendant 4 h à 37 degrés et avec Brefeldin A (10 ug/mL) pendant les 3 dernières heures, comme décrit précédemment14. Les cellules ont d'abord été colorées pour l'antigène de surface avec l'anticorps CD3 PerCP, fixées et après perméabilisation avec la solution perméabilisante BD FACS 2 (BD Biosciences) colorées pour l'anti-IFN-PE (Becton Dickinson). L'IFN intracellulaire est exprimé en pourcentage dans les PBL, ainsi que dans les lymphocytes T CD3.
ELISA.
Les concentrations d'IFN-, d'IL-6 et de TNF dans les sérums des participants étudiés ont été déterminées par des kits ELISA commerciaux non enrobés, conformément aux instructions du fabricant (Invitrogen). Les concentrations de cytokines ont été déterminées aux points 1 (avant la vaccination), au point 3 (1 mois après la primo-immunisation) et au point 4 (2 mois après la primo-immunisation). En bref, les plaques ELISA ont été recouvertes d'anticorps de capture appropriés dans un tampon de revêtement et incubées pendant la nuit à 4 degrés. Tout d’abord, les plaques ont été lavées et bloquées avec le diluant ELISA/ELISAASPOT. Après une heure d'incubation, les plaques ont été lavées et des échantillons de sérum et des standards ont été ajoutés aux puits. Après incubation, lavage et aspiration, conformément aux instructions du fabricant, la solution d'anticorps de détection a été ajoutée à chaque puits. Ensuite, les plaques ont été lavées et aspirées ; la solution d'avidine-HRP a été ajoutée aux puits et incubée pendant 30 min. Ensuite, les plaques ont été lavées et une solution de (3,3′,5,5′-tétraméthylbenzidine) TMB a été ajoutée à chaque puits. Les plaques ont été incubées pendant 15 minutes à température ambiante et la réaction enzymatique a été interrompue par l'ajout d'une solution d'arrêt. L'absorbance a été mesurée à 450/520 nm à l'aide du lecteur de plaques Multiskan EX Termo Labsystems15. Analyses statistiques. Les résultats sont présentés sous forme de valeurs individuelles avec erreur type de la moyenne (SEM). Les différences entre les valeurs ont été comparées à l'aide d'un test t non apparié et d'un test de rang signé de Wilcoxon et les résultats ont été considérés comme statistiquement significatifs si p<0.05. The analysis was performed using GraphPad Prism 9.0 (GraphPad, La Jolla, CA, USA).

cistanche tubulosa-améliorer le système immunitaire
Résultats
3.1 Participants à l'étude et traitement du sérum/lait.
Les caractéristiques des participants à l'étude sont présentées dans le tableau 1. Parmi 61 volontaires ayant reçu le vaccin à ARNm anti-SRAS-CoV-2 BNT162b2, un total de 344 échantillons de sérum ont été collectés à 6 moments précis, à partir de la ligne de base pré-vaccination. à 6 mois après le premier point de vaccination. La plupart des participants à l’étude (97 %) ont signalé des effets indésirables locaux à la vaccination sous la forme de légères douleurs et fatigue aux bras/épaules, qui ont duré 1 à 2 jours. Seuls trois participants ont reçu la deuxième dose de vaccin avec retard, deux en raison d'effets indésirables lors de la primo-vaccination (éruption cutanée, allergie) et un en raison d'un diagnostic de grossesse après la première dose. Aucune infection n’a été signalée entre les deux doses de vaccin. Après six mois de suivi, seuls 3 (5 %) des participants étaient infectés par le SRAS-CoV-2, et aucune forme grave de maladie nécessitant une hospitalisation n'a été détectée. Sept participantes sont tombées enceintes après la vaccination, une 2 semaines après la première dose, une 4 mois après la première dose et 5 plus de 12 mois après la première dose. Le suivi à long terme autodéclaré n'a révélé aucun effet indésirable lié à la vaccination jusqu'à deux ans après la première dose, chez les femmes qui allaitent ou chez tout autre participant à l'étude.
Quantification des anticorps spécifiques du SRAS‑CoV‑2 RBD dans le sérum et le lait des participants à l’étude.
En analysant les niveaux d'anticorps IgG anti-RBD post-vaccination dans le sérum, une augmentation significative des niveaux d'IgG anti-RBD a été observée même 14 jours après la première dose de vaccin dans l'ensemble du groupe analysé par rapport aux niveaux d'IgG avant la vaccination (17,47 ± 51,49 UA). /mL contre 7 828,28 ± 24 157,29 UA/mL, p<0.0001) (Fig. 1a). Te serum levels of anti-RBD IgG continued to rise to 2 months post-vaccination, when a decrease was detected, which lasted up to 6 months, steadily. The levels of anti-RBD IgG antibodies were compared at each time point between naïve and previously infected individuals (Fig. 1b-c), and it was determined that the difference was statistically significant at baseline (point 1), as previously infected individuals had a higher level of antibodies before vaccination (7.23±0.77 AU/mL vs. 54.47±101.40 AU/mL, p<0.01). The difference was statistically significant also in points 2 (3979.48±3277.27 AU/mL vs. 22,581.99±49,570.63 AU/mL, p<0.05), 5 (2369.16±1934.31 AU/ mL vs. 6366.83±6875.85 AU/mL, p<0.01), and 6 (461.96±375.41 AU/mL vs. 766.04±317.35 AU/mL, p<0.05). The decline in antibody levels had the same dynamics in both groups but remained at higher levels in previously infected individuals for up to 6 months. No other analyzed parameters were correlated with a significantly different level of antibodies in serum (age, gender, smoking status). When comparing levels of anti-RBD IgG antibodies in other participants and breastfeeding women (Fig. 1d-e), no significant differences in serum antibody levels were observed in any of the comparisons. Anti-RBD IgG antibodies were also detected in the milk of 4 breastfeeding women (Fig. 1f). In lower levels, they presented with the same dynamics of rising and decline as detected in the serum. Comparing the levels of anti-RBD IgG antibodies in milk at each time point to baseline, (Fig. 1f), it was determined that the difference was statistically significant at points 2 (6.57±0.77 AU/mL vs. 152.13±35.83 AU/ mL, p<0.01) and 6 (6.57±0.77 AU/mL vs. 117.31±25.64 AU/mL, p<0.01).
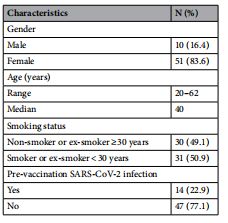
Tableau 1. Caractéristiques des participants à l'étude.

Figure 1. Taux sériques d'anticorps IgG anti-RBD dans (a) l'ensemble du groupe analysé, (b naïfs, c) les individus précédemment infectés, (d) l'ensemble du groupe sans femmes qui allaitent, (e) les femmes qui allaitent et (f) dans le lait des femmes qui allaitent. Les résultats sont présentés sous forme de valeurs individuelles avec erreur type de la moyenne (SEM) de trois répétitions indépendantes. Les différences entre les valeurs ont été comparées à l'aide d'un test t non apparié et les résultats ont été considérés comme statistiquement significatifs si p<0.05. * p<0.05; **p<0.01; *** p<0.0001.
Analyses cytométriques en flux et IFN intracellulaires.
Les données obtenues par analyse cytométrique en flux ont montré que l'expression de CD28 sur les lymphocytes T CD4+ dans le sang périphérique 2 mois après la deuxième dose de vaccin était significativement plus élevée par rapport aux valeurs avant la vaccination (42,84 ± 5,37 % contre 37,75). ±5,96%,p<0.05, Wilcoxon signed-rank test) (Fig. 2a). Tere was a signifcant increase (p≤0.05, Wilcoxon signed rank test) in the prevalence of B cell lymphocyte subset (CD19+) from 6.87±1.17% to 8.73±1.54%, two months afer revaccination, as well as an increased percentage of CD80+ B cells from 1.72±0.28% to 1.99±0.28% (Fig. 2b). Furthermore, fve weeks afer revaccination, a signifcant (p≤0.05, Wilcoxon signed rank test) increase in the percentage of CD14+CD80+ cells from 1.15±0.38% to 5.87±0.95% was detected in the monocyte gate (Fig. 2c). Te expression of IFN-γ in PBLs, as well as in CD3+ T cells was signifcantly (p < 0.05, Wilcoxon signed rank test) increased at 1 week afer the second vaccine dose (1.84 ± 0.13% in PBL and 1.32 ± 0.10% in CD3+ T cells) compared to pre-vaccination baseline values (0.88 ± 0.13% in PBL and 0.72 ± 0.12% in CD3+ T cells) (Fig. 3a). Furthermore, serum levels of IFN-γ were signifcantly increased in all participants from the initial value of 16.69±0.29 pg/mL to 17.72±0.41 pg/mL (p<0.05, Wilcoxon signed rank test) (Fig. 3b), as well as in naive from 16.55±1.77 pg/mL to 17.26±2.53 pg/mL and in a group and previously infected individuals, from 15.93±2.01 pg/mL to 19.90±4.32 pg/mL at 1 week afer revaccination (Fig. 3c). Tere was no signifcant (p>0.05, test de classement signé de Wilcoxon) différence dans les taux sériques d'IL-6 et de TNF- 1 semaine et cinq semaines après la deuxième dose de vaccin par rapport aux valeurs pré-vaccination dans l'ensemble groupe, ainsi que chez les individus naïfs ou précédemment infectés (Fig. Supplémentaire 1a – d).
Discussion
L'épidémie d'infection respiratoire par le SRAS-CoV-2 a eu un effet négatif profond sur divers aspects de la vie quotidienne, notamment sur des problèmes sociétaux, éducatifs et liés à la santé sans lien direct avec la maladie COVID-19 elle-même16-18. . Une approche vaccinale mondiale était nécessaire pour compléter les mesures de distanciation dans la lutte contre la maladie, et de nombreuses études ont exploré l'efficience et l'efficacité de divers types de vaccins distribués dans le monde en 2021. En Serbie, seuls des rapports intermédiaires sur l'immunité humorale 2 et 3 mois après la vaccination sont actuellement disponibles19. ,20 et sont conformes aux données rapportées dans cette étude. Dans notre cohorte analysée jusqu'à 6 mois après la vaccination, un taux de séroconversion de 100 % a été détecté après la première dose de vaccin. Seuls 5 % des participants ont dû recevoir la deuxième dose de vaccin avec retard. Aucun cas d'infection par le SRAS-CoV-2 n'a été signalé entre deux doses de vaccin. Jusqu'à six mois de surveillance, seuls 5 % des participants ont été infectés, sans qu'il soit nécessaire d'être hospitalisé. Les titres d'anticorps IgG anti-RBD SARS-CoV-2 étaient significativement plus élevés par rapport aux valeurs initiales, même après la première dose de vaccin, ce qui contribue à l'idée selon laquelle l'utilisation du vaccin à ARNm BNT162b2 est une approche efficace pour des réponses humorales rapides contre l'original. souches virales. Les taux sériques d'IgG ont continué à augmenter jusqu'à 2 mois après la vaccination, lorsqu'une diminution constante a été détectée jusqu'à la période analysée de 6 mois. Les individus précédemment infectés présentaient des titres d’IgG plus élevés que les individus naïfs jusqu’à 6 mois, ce qui était le seul facteur contribuant aux différents niveaux d’anticorps. Des anticorps IgG anti-RBD ont également été détectés dans le lait des femmes allaitantes dans notre étude et dans certaines études antérieures21, avec une dynamique de titre correspondante à celle du sérum. Des rapports similaires ont été publiés pour les anticorps IgA après une infection naturelle22. Comme les données disponibles sont actuellement limitées sur les risques et les bénéfices de la vaccination des femmes allaitantes, ces résultats sont prometteurs à la lumière d'une éventuelle immunisation passive des nourrissons allaités, même après 6 mois de vaccination des mères. Aucune différence significative dans les taux d'anticorps sériques n'a été observée entre les individus naïfs ou précédemment infectés et les femmes allaitantes, renforçant les observations selon lesquelles la réponse aux vaccins anti-SRAS-CoV-2 n'est pas influencée par la lactation. Les recommandations actuelles stipulent que la vaccination doit être envisagée pour toutes les personnes âgées de 6 mois et plus, y compris celles qui sont enceintes ou qui tentent de concevoir maintenant ou à l'avenir et qui allaitent, quel que soit leur statut d'infection au COVID-19 antérieur23. Notre étude contribue au fardeau des preuves24 suggérant qu'il n'y a eu aucun préjudice immédiat pour les femmes allaitantes recevant le vaccin anti-SRAS-CoV-2 ou pour leurs nourrissons allaités. En outre, sept participantes à l’étude sont tombées enceintes après la vaccination, une 2 semaines après la première dose, une 4 mois après la première dose et 5 plus de 12 mois après la première dose. Des entretiens de suivi à long terme récemment menés auprès des participants à l'étude ont confirmé qu'il n'y avait également aucun préjudice imprévu pour les femmes qui allaitaient ou leurs nourrissons allaités, ou tout autre participant, deux ans après avoir reçu le vaccin anti-SRAS-CoV-2.

Figure 2. Pourcentage de (a) lymphocytes T CD3+CD28+ et CD4+CD28+, (b) CD19+ et CD{{6 }}CD80+ Lymphocytes B, (c) CD14+CD80+ monocytes dans le sang périphérique. Les résultats sont présentés sous forme de valeurs individuelles avec moyenne ± erreur type de la moyenne (SEM). Les différences entre les valeurs ont été comparées à l'aide du test de Wilcoxon et les résultats ont été considérés comme statistiquement significatifs si p<0.05. * p<0.05.
L’apparition de nouveaux variants préoccupants ainsi que l’existence de rapports faisant état d’une baisse rapide des taux d’anticorps anti-SRAS CoV-2 après une infection naturelle et une vaccination25 ont soulevé des incertitudes quant au rôle des composants de l’immunité cellulaire. Quelques études explorant la réponse immunologique des individus vaccinés en Serbie n'ont fait état que d'une immunité humorale19,20. Dans cette étude, une expression accrue des récepteurs costimulateurs CD28 sur les lymphocytes T CD4+ et CD80 sur les lymphocytes B a été détectée 2 mois après l’administration de la deuxième dose de vaccin. De plus, l'expression de CD80 sur les monocytes a augmenté 1- mois après la vaccination complète.
La prolifération et la différenciation des lymphocytes T en cellules efectores ou mémoires nécessitent une présentation d'antigènes, une co-stimulation et des cytokines. Les co-stimulateurs des cellules T les mieux défendus sont des paires de molécules, B7-1 (CD80) et B7-2 (CD86). Ils sont généralement exprimés sur les cellules présentatrices d'antigènes (APC) telles que les cellules dendritiques, les cellules B, les macrophages, les monocytes et les cellules T. Leur expression sur les monocytes est également importante pour l’activation des lymphocytes et de l’immunité adaptative26. Les deux principaux récepteurs présents à la surface des lymphocytes T qui se lient au CD80 et au CD86 sont le CD28 et la protéine 4 associée aux lymphocytes T cytotoxiques (CTLA-4). La liaison au CD28 active les lymphocytes et améliore par conséquent la réponse immunitaire27. Les résultats obtenus dans cette étude montrent que les lymphocytes T CD4+ sont activés par les épitopes dérivés de l'antigène S présentés sur les lymphocytes B et les monocytes activés 2 mois après la deuxième dose du vaccin. Diverses données suggèrent que les lymphocytes T CD4 étaient principalement activés après le vaccin à ARNm28,29, alors que dans certaines études, les lymphocytes T CD4 et CD8 seraient également présentés et activés30. Tan et coll. ont récemment observé que 3 mois après la vaccination, la quantité moyenne de cellules T spécifiques de Spike était équivalente à celle détectée chez les patients convalescents à un moment similaire après l'infection par le SRAS-CoV-231. De plus, les composantes de l’immunité adaptative (à la fois chez les personnes précédemment infectées et vaccinées) semblent être régulées de manière indépendante6,32,33 et il existe un manque de corrélation entre la production d’anticorps antiviraux et la fréquence des lymphocytes T. De plus, les vaccins à ARNm actuels provoquent des réponses immunitaires limitées à la protéine Spike. Cependant, le rôle potentiellement protecteur des lymphocytes T spécifiques d’autres protéines structurelles et non structurales devra également être évalué34. L’idée selon laquelle les vaccins polyantigéniques pourraient exercer un plus grand contrôle contre les variantes virales que les vaccins monoantigéniques, comme les vaccins à base de protéine Spike, pourrait avoir une justification solide35,36.

Figure 3. (a) Expression de l'IFN- dans tous les lymphocytes du sang périphérique CD3+ T. Niveau sérique d'IFN- dans l'ensemble (b) du groupe analysé, (c) les individus naïfs et précédemment infectés. Les résultats sont présentés sous forme de valeurs individuelles avec erreur type de la moyenne (SEM). Les différences entre les valeurs ont été comparées à l'aide du test de Wilcoxon et les résultats ont été considérés comme statistiquement significatifs si p<0.05. * p<0.05.
Dans cette étude, des taux accrus d'IFN- ont été détectés dans tous les lymphocytes et dans les lymphocytes T CD3+ 7 jours après la vaccination complète. En outre, une augmentation du taux d'IFN- dans le sérum de tous les individus vaccinés a été observée, à la fois chez les individus naïfs de SRAS-CoV-2 et chez les individus précédemment infectés 7 jours après la vaccination complète. Ainsi, les cellules T spécifiques de Spike induites par le vaccin à base d’ARNm qui produisent en abondance de l’IFN-. L'IFN- est une cytokine clé dotée de propriétés antivirales et il a été démontré qu'elle inhibe la réplication du SRAS-CoV-28. L'élicitation rapide de l'IFN- par le vaccin BNT162b2 démontrée dans cette étude indique une réponse immunitaire favorable des lymphocytes T contre le virus du SRAS-CoV-2. La réaction immunologique déclenchée par le SRAS-CoV-2 comprend également la production de nombreuses cytokines pro-inflammatoires, principalement l'IL-6 et le TNF- et des modifications de leurs niveaux pourraient être associées au pronostic de la maladie. Des cas graves et mortels de COVID-19 ont été signalés chez des personnes présentant des taux de cytokines accrus37. Cependant, dans cette étude, aucune différence significative dans les taux sériques d'IL-6 et de TNF- n'a été détectée 7 jours et jusqu'à 1 mois après la vaccination complète, ce qui pourrait résulter des caractéristiques spécifiques de la cohorte et du moment de l'échantillonnage.
Ces données représentent les premiers rapports publiés sur l'immunité durable prenant en compte à la fois la composante humorale et cellulaire, et se concentrant sur les femmes qui allaitent. Cela pourrait être particulièrement utile pour les futures méta-analyses de ce sous-groupe et d’autres sous-groupes de population sensibles, car les données de la région des Balkans sur la population slave sont généralement absentes des efforts multinationaux plus vastes.

cistanche tubulosa-améliorer le système immunitaire
Conclusions
Le vaccin anti-SARS-CoV-2 BNT162b2 à ARNm a induit des réponses humorales et cellulaires mesurables et durables chez les femmes qui allaitent et chez les individus naïfs et précédemment infectés au cours des six premiers mois suivant la vaccination en Serbie. Aucun effet indésirable grave lié à la vaccination n'a été signalé et seulement 5 % des participants ont été infectés par le SRAS-CoV-2 au cours des six premiers mois suivant la vaccination, sans qu'il soit nécessaire d'être hospitalisé. Aucun préjudice imprévu n'a été signalé pour les femmes qui allaitent ou leurs nourrissons allaités deux ans après avoir reçu le vaccin anti-SRAS-CoV-2. Les prochaines études dans ce domaine devraient se concentrer sur les stratégies de recherche et de développement de vaccins qui pourraient maintenir le COVID-19 et d'éventuelles pandémies similaires sous un contrôle plus rapide et durable. Des efforts doivent également être déployés pour fournir des lignes directrices fondées sur des connaissances, lutter efficacement contre la désinformation, en particulier concernant les sous-populations sensibles telles que les femmes qui allaitent, faciliter l’accès aux vaccins en période de besoin élevé et renforcer la confiance générale dans la science.

avantages cistanche-renforcer le système immunitaire
Les références
1. OMS, Tableau de bord de l'OMS sur le coronavirus (COVID-19) de l'Organisation mondiale de la santé. https://covid19.who.int/ (2022).
2. Hojyo, S. et al. Comment le COVID-19 provoque une tempête de cytokines avec une mortalité élevée. Infamme. Régénération. 40, (2020).
3. van Eeden, C., Khan, L., Osman, MS & Tervaert, JWC Dysfonctionnement des cellules tueuses naturelles et son rôle dans le COVID-19. Int. J. Mol. Sci. 21, 6351 (2020).
4. Sette, A. & Crotty, S. Immunité adaptative contre le SRAS-CoV-2 et le COVID-19. Cellule 184, 861-880 (2021).
5. Chen, G. et coll. Caractéristiques cliniques et immunologiques de la maladie à coronavirus sévère et modérée 2019. J. Clin. Investir. 130, 2620-2629 (2020).
6. Dan, JM et coll. Mémoire immunologique au SRAS-CoV-2 évaluée jusqu'à 8 mois après l'infection. Sciences 80, 371 (2021).
7. Turner, JS et coll. Les vaccins à ARNm du SRAS-CoV-2 induisent des réponses persistantes du centre germinal humain. Nat. 596, 109-113 (2021).
8. Peintre, MM et al. L'induction rapide de lymphocytes T CD4+ spécifiques à l'antigène est associée à une immunité humorale et cellulaire coordonnée contre la vaccination par ARNm du SRAS-CoV-2. Immunité 54, 2133-2142.e3 (2021).
9. Goel, RR et coll. La vaccination par ARNm induit une mémoire immunitaire durable contre le SRAS-CoV-2 avec une évolution continue vers des variantes préoccupantes. bioRxiv Prépr. Servir. Biol. https://doi.org/10.1101/2021.08.23.457229, (2021)
10. Muyldermans, J., De Weerdt, L., De Brabandere, L., Maertens, K. & Tommelein, E. Les effets de la vaccination covid-19 sur les femmes allaitantes : une revue systématique de la littérature. Devant. Immunol. 13, 1498 (2022).
11. Golan, Y. et coll. Vaccination à ARNm Covid-19 pendant l'allaitement : évaluation des événements indésirables et des anticorps liés au vaccin dans les dyades mère-enfant. Devant. Immunol. 12, 777103 (2021).
12. Arbeitman, CR et coll. Comparaison structurelle et fonctionnelle du domaine de liaison du récepteur de pointe du SRAS-CoV-2- produit dans Pichia pastoris et dans les cellules de mammifères. Sci. Rep.10, 21779 (2020).
13. Konjevic, G. et al. Évaluation de la capacité fonctionnelle des cellules NK de patients atteints de mélanome dans un modèle in vitro de contact de cellules NK avec des lignées cellulaires tumorales K562 et femx. J.Membre. Biol. 250, 507-516 (2017).
14. Konjevic, G. et al. La diminution de l'activation du CD161 et l'augmentation de l'expression du récepteur inhibiteur du CD158a sur les cellules NK sont à l'origine d'une cytotoxicité altérée des cellules NK chez les patients atteints de myélome multiple. J. Clin. Pathol. https://doi.org/10.1136/jclinpath-2016-203614 (2016).
15. Stanojković, TP et al. Évaluation de l'expression des cytokines et des sous-ensembles de cellules immunitaires circulantes en tant que paramètres potentiels de la toxicité aiguë des radiations chez les patients atteints d'un cancer de la prostate. Sci. Rep.10, 19002 (2020).
16. Cavic, M. et coll. Explorer l'effet réel de la pandémie de SRAS-CoV-2 sur le diagnostic moléculaire des patients atteints de cancer et des personnes à haut risque. Expert Révérend Mol. Diagnostic. 21, 101-107 (2021).
17. Hassan, I., Mukaigawara, M., King, L., Fernandes, G. et Sridhar, D. Le recul est-il en 2020 ? Leçons de gouvernance mondiale de la santé un an après le début de la pandémie. Nat. Méd. 27, 396-400 (2021).
18. Cavic, M., Grahovac, J., Zec, R., Stefanovic, M. & Aleksic, E. Aperçu de la première année de la pandémie de SRAS-CoV-2 en Serbie et dans le comté de Pirot. Pirot. Zb. 46, 1–23 (2021).
19. Lijeskić, O. et al. Une étude de cohorte prospective sur la cinétique d'anticorps spécifiques contre l'infection par le SRAS-CoV-2 et contre quatre vaccins contre le SRAS-CoV-2 disponibles en Serbie, et l'efficacité du vaccin : un rapport intermédiaire de 3-mois. Vaccins 9, (2021).
20. Petrović, V., Vuković, V., Patić, A., Marković, M. & Ristić, M. Immunogénicité des vaccins BNT162b2, BBIBP-CorV et Gam-COVID-Vac et immunité après le SRAS-CoV naturel{{7 }} infection-Une étude comparative de Novi Sad. Serbie. PLoS One 17, e0263468 (2022).
21. Yeo, KT et coll. Activité neutralisante et persistance de l'ARNm du vaccin SRAS-CoV-2 dans le sérum et le lait maternel après la vaccination BNT162b2 chez les femmes allaitantes. Devant. Immunol. 12, (2022).
22. Pace, RM et coll. Le lait des femmes diagnostiquées avec le COVID-19 ne contient pas d'ARN du SRAS-CoV-2 mais présente des niveaux persistants d'anticorps IgA spécifiques au SRAS-CoV-2-. Devant. Immunol. 12, 5566 (2021).
23. CDC, C. pour les vaccins DC et P. COVID-19 pendant la grossesse ou l'allaitement. https://www.cdc.gov/coronavirus/2019-ncov/vacci nes/recommendations/pregnancy.html (2022).
24. Bethesda (MD), NI de CH et HD Base de données sur les médicaments et la lactation (LactMed). Vaccins contre la COVID-19. (2022).
25. Jo, DH et coll. Diminution rapide des titres d'anticorps contre le SRAS-CoV-2 dans les 4 mois suivant la vaccination BNT162b2. Vaccins 9, (2021).
26. Carreno, BM & Collins, M. Famille de ligands Te B7 et ses récepteurs : nouvelles voies de costimulation et d'inhibition des réponses immunitaires. Ann. Révérend Immunol. 20, 29-53 (2002).
27. Esensten, JH, Helou, YA, Chopra, G., Weiss, A. & Bluestone, JA Costimulation CD28 : du mécanisme à la thérapie. Immunité 44, 973-988 (2016).
28. Geers, D. et coll. Les variantes préoccupantes du SRAS-CoV-2 échappent partiellement aux réponses humorales, mais pas aux lymphocytes T, chez les donneurs convalescents et les vaccinés du COVID-19. Sci. Immunol. 6, (2021).
29. Tarke, A. et coll. Impact des variantes du SRAS-CoV-2 sur la réactivité totale des lymphocytes T CD4 + et CD8 + chez les individus infectés ou vaccinés. Rapports de cellules. Méd. 2, (2021).
30. Sahin, U. et al. Le vaccin BNT162b2 induit des anticorps neutralisants et des cellules T poly-spécifiques chez l’homme. Nat. 2021 5957868 595, 572-577 (2021).
31. Tan, AT et coll. Mesure rapide des lymphocytes T Spike du SRAS-CoV-2 dans le sang total d'individus vaccinés et naturellement infectés. J. Clin. Investir. 131, (2021).
32. Chia, WN et al. Dynamique des réponses en anticorps neutralisants du SRAS-CoV-2 et durée de l’immunité : une étude longitudinale. Te Lancet Microbe 2, e240 – e249 (2021).
33. Reynolds, CJ et coll. Réponses discordantes des anticorps neutralisants et des lymphocytes T dans les infections asymptomatiques et légères par le SRAS-CoV-2. Sci. Immunol. 5, (2020).
34. Lopandić, Z. et al. IgM et IgG Immunoréactivité de la protéine m recombinante du SRAS-CoV-2. Int. J. Mol. Sci. 22, (2021).
35. Altmann, DM, Boyton, RJ et Beale, R. Immunité aux variantes préoccupantes du SRAS-CoV-2. Sciences 371, 1103-1104 (2021).
36. Matchett, WE et coll. À la pointe de la technologie : le vaccin Nucleocapsid suscite une immunité protectrice contre le SRAS-CoV-2 indépendante des pointes. J. Immunol. 207, 376-379 (2021).
37. Costela-Ruiz, VJ, Illescas-Montes, R., Puerta-Puerta, JM, Ruiz, C. & Melguizo-Rodríguez, L. Infection par le SRAS-CoV-2 : le rôle des cytokines dans le COVID{{ 7}} maladie. Facteur de croissance des cytokines Rév. 54, 62 (2020).
