Comment Apelin-13 soulage-t-il efficacement la néphropathie diabétique ?
Mar 18, 2022
Contact:joanna.jia@wecistanche.com/ Whatsapp : 008618081934791
L'apéline-13 atténue la néphropathie diabétique en améliorant la production d'oxyde nitrique et en supprimant la fibrose des tissus rénaux
ZHUO GAO, XIN ZHONG, YING-XIA TAN & DONG LIU
Résumé
Le diabète est une maladie métabolique grave, et les lésions rénales induites par le diabète affectent également gravement la survie des patients. L'apeline est une molécule qui joue un rôle crucial dans le métabolisme des lipides, et des études récentes ont révélé queapelin-13, un sous-type d'apéline, joue un rôle important dans la régulation de la glycémie. Cependant, le rôle deapelin-13dansnéphropathie diabétiquereste pas clair. Dans la présente étude, un modèle de rat dediabétiquenéphropathiea été construit par injection de streptozocine (STZ). Au cours de ce processus, ces rats ont reçu une injection deapelin-13. La glycémie, les protéines urinaires et les taux d'insuline ont été déterminés chaque semaine. Ensuite, l'expression de la protéine associée au récepteur de type 1 du domaine de l'angiotensine (APJ), de la synthase de l'oxyde nitrique endothélial (eNOS), de la E-cadhérine et de l'actine musculaire lisse (a-SMA) dans les tissus rénaux a été déterminée par Western blot. Ensuite, les cellules endothéliales des vaisseaux glomérulaires ont été cultivées avec un milieu riche en glucose. Ces cellules ont été traitées avecapelin-13pendant 24h. Enfin, la viabilité cellulaire de ces cellules et l'expression de l'APJ, de l'eNOS.E-cadhérine et de la -SMA dans ces cellules ont été déterminées par Western blot. En conséquence, le traitement deapelin-13induit des niveaux inférieurs de glucose sanguin et de protéines urinaires. De plus, l'application deapelin-13favorise la production d'insuline et atténue la résistance à l'insuline. Traitement avecapelin-13a favorisé l'expression de l'APJ, de l'eNOS et de la E-cadhérine tout en supprimant l'expression de -SMA dans les tissus rénaux des rats et les cellules endothéliales des vaisseaux glomérulaires. Par ailleurs, l'application deapelin-13également favorisé la viabilité cellulaire de ces cellules. En conclusion,apelin-13soulagédiabétiquenéphropathieen favorisant la production d'oxyde nitrique (NO) et en atténuant la fibrose des tissus rénaux.

Introduction
Le diabète est une maladie métabolique et le trouble du métabolisme du glucose en est la principale manifestation clinique(1). Des études antérieures ont indiqué qu'en raison de la popularité des régimes riches en sucre et en matières grasses et du mode de vie sédentaire des individus, l'incidence du diabète devrait continuer d'augmenter au cours des prochaines années(2.,3). L'apparition du diabète s'accompagne souvent de lésions de plusieurs organes et les patients atteints de diabète de longue durée reçoivent souvent un diagnostic d'insuffisance rénale sévère (4,5). Une étude précédente a rapporté que 30 % des patients atteints de diabète de type 1 et 25 % des patients atteints de diabète de type 2 ont développédiabétiquenéphropathie(6). En outre, l'apparition et le développement dediabétiquenéphropathieconduit à une augmentation de la mortalité des patients diabétiques.Diabétiquenéphropathie-les lésions rénales induites par les podocytes et les capillaires sont le principal facteur affectant la survie des patients(7). Par conséquent, le développement d'un traitement pourdiabétiquenéphropathieest crucial pour améliorer le taux de survie des patients diabétiques.
L'apeline est située dans la région chromosomique Xq25-26.1 et codée par le gène APLN (8). généralement sécrétée et produite par le tissu adipeux blanc (9). L'apeline et son récepteur APJ sont largement exprimés dans divers tissus, y compris les cellules endothéliales cérébelleuses, le cœur et les vaisseaux sanguins, en particulier dans le système cardiovasculaire (10). L'apeline a été identifiée comme une adipokine associée au métabolisme des lipides dans une étude récente(11). Cependant, une étude antérieure a indiqué que l'apéline joue un rôle crucial dans la régulation de l'homéostasie énergétique du corps, du métabolisme du glucose et de l'eau ainsi que d'autres fonctions biologiques(12). L'expression de l'apeline a déjà été révélée pour améliorer la résistance à l'insuline, l'athérosclérose et les dommages vasculaires induits par le diabète (13). Cependant, une étude différente a révélé que l'expression de l'apéline induisait l'apparition et le développement de la rétinopathie diabétique (14). Par conséquent, le rôle de l'apéline dans la survenue et le développement de complications liées au diabète reste incertain.
De plus, l'apéline est présente sous différents sous-types (apéline-36, apéline-17 etapelin-13) dans le corps par le cisaillement du réticulum endoplasmique. Il a été révélé que plus la chaîne peptidique de l'apeline est courte, plus son activité biologique est forte(15). Une étude précédente a indiqué que l'apéline améliorait la sensibilité à l'insuline et induisait une baisse de la glycémie en réduisant l'inflammation chronique chez les patients atteints de diabète de type 2, améliorant ainsi le métabolisme du glucose et des lipides (16). Cependant, l'effet de l'apéline surdiabétiquenéphropathiefait actuellement polémique. Une étude précédente a rapporté que les taux d'apéline/APJ dans le sérum de patients atteints dediabétiquenéphropathiesont élevés, favorisant l'apparition et le développement dediabétiquenéphropathie(17). D'autre part, une étude différente a révélé queapelin-13pourrait inhiber les changements morphologiques des cellules épithéliales tubulaires rénales dans l'environnement riche en glucose, inhibant ainsi l'apparition et le développement du processus de transition épithéliale-mésenchymateuse (EMT) dans les cellules glomérulaires, et retardant finalement l'apparition dediabétiquenéphropathie(18). Par conséquent, l'effet de l'apéline sur les complications rénales induites par le diabète reste incertain.
Dans la présente étude, le rôle deapelin-13dans le processus dediabétiquenéphropathiea été étudiée plus avant en construisant un modèle de rat dediabétiquenéphropathie.

Cistanchetubuleuxempêcheun reinmaladie, cliquez ici pour obtenir l'échantillon
matériaux et méthodes
Essais sur animaux. Un total de 30 rats mâles Sprague Dawley (âgés de 6-8semaines ;200-230g) ont été obtenus auprès du Beijing Vital River Laboratory Animal Technology Co.Ltd. et logé dans une pièce à température contrôlée (25 degrés) et exempte d'agents pathogènes spécifiques avec une humidité constante (40-50 pour cent) dans un cycle lumière/obscurité de 12-h et a reçu de la nourriture et de l'eau à volonté pendant une semaine . Ces rats ont ensuite été divisés en six groupes (contrôle, modèle, Ap-E40, Ap-E400, Ap-L40 et Ap-L400). Les rats du groupe témoin ont été traités sans rien. Les rats des autres groupes ont été nourris avec un régime riche en sucre et en graisses (Thermo Fisher Scientific, Inc.) et ont reçu une injection intraveineuse de streptozocine (STZ ; 40 mg/kg ; produit n° S0130 ; Merck KGaA) tous les la semaine. Après 3 semaines, les rats Ap-E40 et Ap-E400 ont été traités avecapelin-13(40 et 400 pmol/kg, respectivement ; produit n° A6469 ; Merck KGaA). Au total 6 semaines après l'injection de STZ, les rats des groupes Ap-L40 et Ap-L400 ont été traités avecapelin-13(40 et 400 pmol/kg, respectivement). Après huit injections de STZ, les rats ont été euthanasiés avec du pentobarbital sodique (160 mg/kg, ip). Après l'euthanasie, le sérum et les organes ont été prélevés. Le poids des rats a été relevé à l'aide de balances électroniques chaque semaine, depuis 1 semaine avant l'injection de STZ et jusqu'à l'euthanasie. Les taux de glucose sanguin ont été détectés chaque semaine à l'aide d'un lecteur de glycémie (Thermo Fisher Scientific, Inc.). Les taux de protéines urinaires ont également été détectés à l'aide d'un kit de dosage BCA (cat.no. P0012S; Beyotime Institute of Biotechnology) chaque semaine. L'insuline sérique à jeun a également été détectée chaque semaine à l'aide d'un kit commercial (cat.no.RAB0904; Merck KGaA) selon les instructions du fabricant. L'indice de résistance à l'insuline a été calculé à l'aide de la formule suivante : (taux d'insuline dans le sang x taux de glycémie)/22,5. Toutes les expériences ont été réalisées conformément au Guide pour le soin et l'utilisation des animaux de laboratoire 8e édition(19) et approuvées (n° d'approbation2020-79-PJO1) par le comité d'éthique du centre médical de l'armée de l'air (Pékin, Chine) .
Détection de l'azote uréique du sang (BUN) et de la créatinine sérique (Ser). Les niveaux de BUN (cat.no.ml076479) et Scr (cat. no.ml059158) dans le sang ont été déterminés à l'aide de kits commerciaux (Shanghai Enzyme-linked Biotechnology Co., Ltd.) après 3 et 8 semaines d'injection de STZ, respectivement . Toutes les étapes de ce dosage ont été réalisées selon les instructions des fabricants.
Détection de l'oxyde nitrique (NO), de l'angiotensine II (Ang Il) et de l'endothéline-1(ET-1). Les niveaux de NO, Ang II et ET-1 dans le sérum et les tissus néphridiaux ont été détectés à l'aide du kit NO (cat.no. S0021 ; Beyotime Institute of Biotechnology), du kit Ang II (produit no. RAB0010 ; Merck KGaA ), et le kit ET-1 (cat.no.E-EL-R1458c ; Elabscience Biotechnology, Inc.). Toutes les étapes des tests ont été effectuées conformément aux instructions du fabricant.
Coloration à l'hématoxyline et à l'éosine (H&E). Après l'euthanasie, les tissus rénaux ont été prélevés et lavés avec une solution saline tamponnée au phosphate (PBS) pré-refroidie. Le rein a ensuite été séparé et fixé avec du paraformaldéhyde à 4 % pendant une nuit à température ambiante. Les tissus rénaux inclus en paraffine ont été coupés en sections de 5- um. Ensuite, ces sections ont été déshydratées dans une solution d'éthanol à 70 et 90 % pendant 10 minutes chacune. Enfin, une coloration H&E à température ambiante pendant 3 min a été réalisée pour détecter les changements pathologiques. Toutes les étapes de ce test ont été effectuées conformément aux instructions du fabricant du kit de coloration H&E (cat.no.C0105S; Beyotime Institute of Biotechnology).
Immunohistochimie. L'immunohistochimie a été réalisée en utilisant la méthode standard à la peroxydase/DAB et la contre-coloration à l'hématoxyline selon les instructions du fabricant. Après avoir été bloquées avec 5 % d'albumine de sérum bovin (BSA ; Beyotime Institute of Biotechnology) pendant 20 min à température ambiante, les coupes ont été incubées avec un anticorps primaire anti-APJ (cat.no.PA5-114830 ;Thermo Fisher Scientific, Inc. . une nuit à 4 degrés. Après lavage au PBS, les coupes ont été incubées avec un anticorps secondaire de chèvre anti-lapin conjugué à la peroxydase de raifort (code produit ab6721 ; 1: 1, 000 ; Abcam) à 4 C pendant 50 min, suivi de la Lavage au PBS Ensuite, les sections ont été traitées avec une solution de DAB et contre-colorées avec de l'hématoxyline à température ambiante pendant 5 minutes Enfin, les images ont été obtenues à l'aide d'un microscope optique (Olympus Corporation).
Culture cellulaire et traitement. Une lignée de cellules endothéliales microvasculaires glomérulaires rénales humaines (hRGEC) a été obtenue auprès de BioVector NTCC, Inc. et cultivée dans un milieu RPMI -1640 (Thermo Fisher Scientific, Inc., complété par 10 % de sérum bovin fœtal (FBS) dans un milieu humidifié air à 37 °C avec 5 % de CO. Ces cellules ont été divisées en groupes contrôle, modèle, Ap-L(Apelin-low) et Ap-H(Apelin-high).Modèle, Ap-L et Ap-H groupe les cellules ont été cultivées dans un milieu RPMI-1640 à haute teneur en glucose (25 mmol/l : Cytiva) et les cellules du groupe témoin ont été cultivées dans un milieu RPMI-1640avec une teneur en glucose normale (5,5 mmol/l). Les cellules du groupe Ap-L ont été traitées avec de faibles niveaux deapelin-13(0.1 μmol/) et les cellules du groupe Ap-H ont été traitées avec des niveaux élevés deapelin-13(1 μmol/).
Expérience de formation de tubes. La formation de tubes dans les cellules hRGEC a été déterminée à l'aide d'un kit commercial (produit n° K905-50 ; AmyJet Scientific, Inc). Toutes les images ont été obtenues à l'aide d'un microscope optique (grossissement x4 ; Olympus Corporation). Toutes les étapes de ce dosage ont été réalisées selon les instructions du fabricant.
Kit de comptage de cellules-8(CCK-8). Les cellules hRGEC de différents groupes ont été étalées dans trois 96-plaques à puits (2,5 x 104/puits). Après 24, 48 et 72 h d'incubation à 37 degrés, 10 ul de réactif CCK-8 (Dojindo Molecular Technologies, Inc.) ont été dilués avec le milieu de culture et ajoutés aux plaques à puits 96-. Ensuite, ces cellules ont été placées dans un incubateur pendant 1 h. Pour terminer. l'absorbance de ces cellules a été détectée à l'aide d'un spectrophotomètre (Thermo Fisher Scientific, Inc.) à une longueur d'onde de 450 nm.
Western blot. Les protéines totales ont été recueillies à partir de tissus néphridiaux et de cellules hRGEC à l'aide d'un tampon de lyse RIPA (Santa Cruz Biotechnology, Inc.). La concentration en protéines a été déterminée à l'aide d'un kit de dosage BCA. Ensuite, des quantités égales de protéines (40 ugs) ont été séparées par électrophorèse sur gel de polyacrylamide-dodécylsulfate de sodium à 10 % (SDS-PAGE) (Beyotime Institute of Biotechnology) et transférées sur une membrane de fluorure de polyvinylidène (PVDF) (EMD Millipore). qui a été bloqué avec 5 pour cent d'albumine de sérum bovin (BSA) (Beyotime Institute of Biotechnology) à 37 degrés pendant 1,5 h. Les membranes ont ensuite été incubées avec les anticorps primaires suivants à 4 degrés pendant la nuit : récepteur de l'Ang II de type 1 (AT1R : 1 : 1,000 ; code produit ab124734 ; Abcam), NO synthase endothéliale (eNOS ; 1 : 1, 000 ; code produit ab5589 ; Abcam), APJ(1:1,000;cat.no.PA5-114830 ; Thermo Fisher Scientific, Inc), récepteur du facteur de croissance transformant (TGBR : 1:1.000;code produit ab97459 ; Abcam), E-cadhérine (1:1,000 :code produit ab212059 ; Abcam), -actine musculaire lisse( -SMA;1:1. 000 : produit n° 19245 ; Cell Signaling Technology, Inc.) et GAPDH (1:2 500 ; code produit ab9485 ; Abcam). Après l'incubation de l'anticorps primaire, les membranes ont été lavées avec du PBS-Tween-20(0,1 %) et incubées avec un anticorps conjugué à la HRP (1:2,000 ; code produit ab6721 ; Abcam) pendant 2 h à température ambiante(7)Enfin, les signaux immunoréactifs ont été évalués à l'aide d'un kit Pierce ECL Western Blotting Substrate (Thermo Fisher Scientific, Inc.) selon les instructions du fabricant. Les intensités relatives des immunoblots ont été mesurées avec un imageur moléculaire Versa Doc MP 5000 et le logiciel Quantity One (version 4.6) (tous deux de Bio-Rad Laboratories, Inc.).
Analyses statistiques. L'analyse statistique a été effectuée à l'aide de Graph Pad Prism 7.0(GraphPad Software, Inc.). Des tests t de Student non appariés ont été utilisés pour comparer deux groupes. Les comparaisons entre les différents groupes ont été évaluées à l'aide d'une ANOVA à un facteur suivie du test posthoc de Tukey. Toutes les données sont présentées sous forme de moyenne ± écart type (SD) et toutes les expériences ont été répétées trois fois. P<0.05 was="" considered="" to="" indicate="" a="" statistically="" significant="">

Résultats
Apéline-13diminue le poids et la glycémie et augmente les niveaux d'insuline dediabétiquenéphropathierats à 8 semaines. Le poids et la glycémie des rats ont été détectés chaque semaine au cours du processus d'élevage. Les résultats (Fig.1A et B) ont révélé que le poids et la glycémie des rats des groupes Ap-E40 et Ap-E400 n'étaient pas significativement modifiés après l'injection deapelin-13à 3 semaines. Les mêmes paramètres chez les rats des groupes Ap-L40 et Ap-L400 ont été diminués aprèsapelin-13injection à 8 semaines par rapport à celle à 3 semaines. Les niveaux d'insuline dans le sang ont également diminué après laapelin-13injection à 8 semaines par rapport à celle à 3 semaines (Fig.1C).
Apéline-13la thérapie améliore la fonction rénale dediabétiquenéphropathieles rats. L'augmentation des niveaux d'azote uréique et de Scr a indiqué la survenue et le développement d'une lésion rénale (20). Les niveaux d'azote uréique et de Scr se sont révélés plus élevés après laapelin-13injection à 8 semaines par rapport à celle à 3 semaines (Fig. 2A). De même, la teneur en protéines urinaires et l'étendue des lésions pathologiques des tissus rénaux ont également révélé les mêmes tendances (Fig.2B et C).
Apéline-13atténuediabétiquenéphropathieen modulant la production de NO, Angel et ET-1. L'expression de l'APJ a été détectée et les résultats (Fig.3A) ont révélé que l'expression de l'APJ dans les tissus rénaux des rats était diminuée après laapelin-13injection à 8 semaines par rapport à celle à 3 semaines. AUCUNE production ne pourrait soulager lediabétiquenéphropathie-dommages vasculaires induits dans le tissu rénal (21). Par conséquent, la production de NO, Ang II et ET-1 a été détectée dans les tissus rénaux. Les résultats ont révélé que les niveaux de NO étaient diminués après l'injection deapelin-13à 8 semaines par rapport à celle à 3 semaines. Cependant, les niveaux d'Ang II et d'ET-1 ont augmenté après l'injection deapelin-13à 8 semaines par rapport à celle à 3 semaines (Fig.3B et C). Ensuite, l'expression de eNOS et AT1R a été détectée par western blot. Comme le révèle la Fig.4A, l'expression de AT1R a été supprimée après l'injection deapelin-13à 3 et 8 semaines par rapport au groupe modèle, respectivement. Les niveaux d'eNOS ont augmenté après l'injection deapelin-13à 3 et 8 semaines par rapport au groupe modèle.
Apéline-13atténuediabétiquenéphropathieen modulant l'expression de l'ATIR, de l'eNOS nitrique endothéliale et des protéines liées à la fibrose rénale dans la voie APJ. L'expression d'APJ a été augmentée et celle de TGBR a été diminuée après l'injection deapelin-13à 3 et 8 semaines par rapport au groupe modèle. Les niveaux d'expression des protéines liées à la fibrose, E-cadhérine et -SMA, ont été détectés, et les résultats ont révélé que l'expression de la E-cadhérine était améliorée et que les niveaux d'a-SMA étaient diminués après l'injection deapelin-13à 3 et 8 semaines par rapport au groupe modèle (Fig. 4B).
Apéline-13favorise la prolifération et la formation de tubes et module l'expression des protéines liées à la fibrose rénale dans la voie APJ dans les cellules endothéliales vasculaires rénales induites par une glycémie élevée à court terme. Les cellules hRGEC ont été cultivées dans le milieu riche en glucose pendant 24, 48 et 72 h. Ensuite, un test CCK -8 a été effectué pour détecter la viabilité cellulaire. Les résultats (Fig.5A) ont révélé que le traitement avecapelin-13favorise la viabilité cellulaire. L'application deapelin-13a également favorisé la formation de lumen (Fig.5B). A 24h deapelin-13traitement, il a été révélé que les niveaux d'expression de l'APJ, de l'eNOS et de la E-cadhérine étaient augmentés et que les niveaux de TGBR, ATIR et -SMA étaient diminués par rapport au groupe modèle (Fig. 5C).
Apéline-13supprime la prolifération et la formation de tubes et module l'expression des protéines liées à la fibrose rénale dans la voie APJ dans les cellules endothéliales vasculaires rénales induites par une glycémie élevée à long terme. Les cellules ont été traitées avec un milieu riche en glucose pendant 72 et 96 h, et l'interférence avecapelin-13commencé à partir de 72 h. Après 24 h, les résultats du test CCK-8 ont révélé que l'application deapelin-13viabilité cellulaire supprimée par rapport au groupe modèle (Fig.6A). La formation de lumen a été inhibée suite au traitement avecapelin-13(Fig.6B).De plus. traitement avecapelin-13a également favorisé l'expression de l'APJ, de l'eNOS et de la E-cadhérine par rapport au groupe modèle. L'application deapelin-13a également supprimé l'expression de TGBR, AT1R et a-SMA (Fig.6C) par rapport au groupe modèle de manière dose-dépendante.
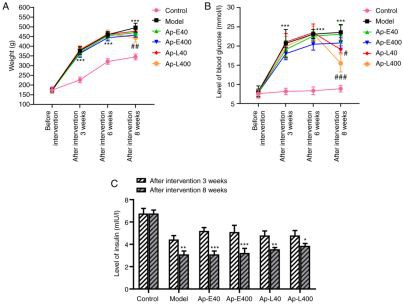 | 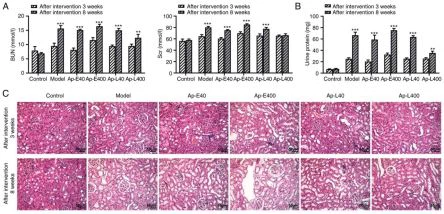 |
| Figure 1. Apelin-13 soulage la résistance à l'insuline des rats.(A) Le poids des souris a été détecté chaque semaine. (B) La glycémie a été détectée chaque semaine. "P-<0.001 vs.the="" control="" group.=""><><0.01 and=""><0.001 vs.the="" model="" group.(c)levels="" of="" insulin="" were=""><0.05,"p-0.01><0.001 vs.the="" after="" intervention="" 3w=""> | Figure 2. Le traitement de l'apeline-13 atténue les lésions rénales induites par le diabète chez les rats.(A) Les niveaux d'azote uréique sanguin et de créatinine sérique ont été détectés. (B) La teneur en protéines urinaires a été détectée chaque semaine. (C) La lésion des tissus rénaux a été détectée avec la coloration à l'hématoxyline et à l'éosine (grossissement.x200), P<0.01, and="" p-0.001="" ys.the="" after="" intervention="" 3w="" group.bun.blood="" urea="" nitrogen:="" scr,="" serum=""> |
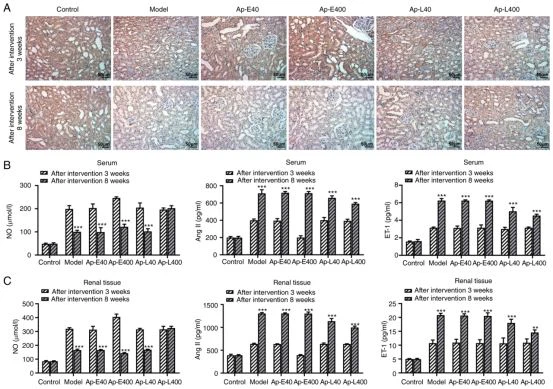 | 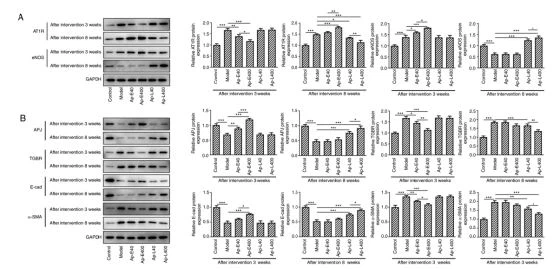 |
| Figure 3. Apelin-13 active l'expression de APJ.(A) L'expression de l'APJ dans les tissus rénaux a été détectée avec les tests immunohistochimiques (grossissement, x200). (B) La production de NO a été détectée avec les kits commerciaux. (C) Les niveaux d'Ang Il et d'ET-I ont été déterminés avec des kits commerciaux."P<0.01><0.001 vs.="" the="" after="" intervention="" 3w="" group.apj,="" angiotensin="" domain="" type="" 1="" receptor-associated="" proteins;="" no,="" nitric="" oxide;="" ang="" i,="" angiotensin="" ii;=""> | Figure 4. L'application d'apelin-13 favorise l'expression d'eNOS.(A) L'expression d'ATIR et d'eNOS a été détectée avec le western blot. (B) Les niveaux d'APJ, de TGBR, de E-cadhérine et d'a-SMA dans les tissus rénaux de rats ont été détectés par Western blot.'P<><0.01><0.001.enos, endothelial="" nitric="" oxide="" synthase;="" at1r,="" ang="" ii="" type="" i="" receptor;="" apj,="" angiotensin="" domain="" type="" 1="" receptor-associated="" proteins;="" tgbr,="" transforming="" growth="" factorβreceptor;="" α-sma,="" α-smooth="" muscle=""> |
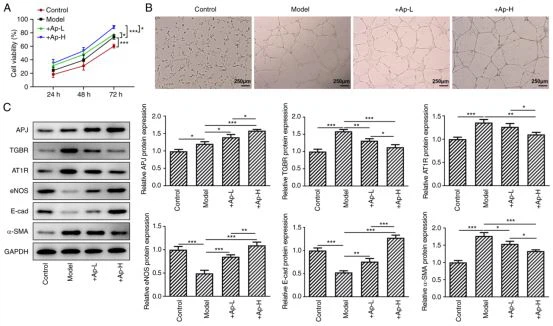 | 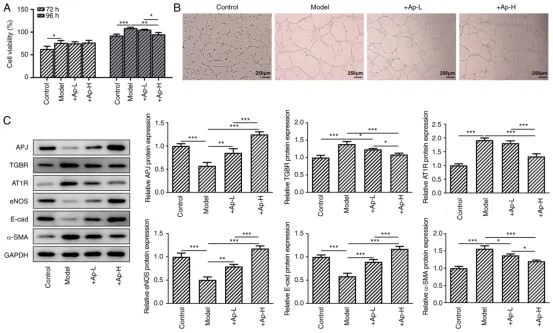 |
| Figure 5.Apelin-13 atténue les lésions induites par le glucose plus élevées des cellules endothéliales des vaisseaux glomérulaires.(A) La viabilité cellulaire a été détectée avec le kit de comptage de cellules-8. (B) hRGECs ont été détectés avec les expériences de formation lumen (grossissement, x4). (C) L'expression de AT1R.eNOS, APJ, TGBR, E-cadhérine et a-SMA dans ces cellules a été déterminée avec le Western blot,' P-0.05."P<0.01><0.001. atir.="" ang,="" i="" type="" 1="" receptor:="" enos,="" endothelial="" nitric="" oxide="" synthase;="" apj,="" angiotensin="" domain="" type="" i="" receptor-associated="" proteins;="" tgbr,="" transforming="" growth="" factor="" βreceptor;a-sma,α-smooth="" muscle=""> | Figure 6. Apelin-13 soulage la lésion des cellules endothéliales des vaisseaux glomérulaires en supprimant la fibrose.(A) La viabilité cellulaire des cellules endothéliales des vaisseaux glomérulaires a été déterminée avec le test CellCounting Kit -8. (B) Les hRGEC ont été détectés avec les expériences de formation de lumen (grossissement, x4). (C) Les niveaux d'AT1R, d'eNOS, d'APJ, de TGBR.E.-cadhérine et d'a-SMA dans ces cellules ont été déterminés par Western blot."P-<><0.01><0.001.stir. ang="" iitype="" 1receptor;enos,="" endothelial="" nitric="" oxide="" synthase;="" apjangiotensin="" domain="" type="" 1="" receptor-associated="" proteins;="" tgbr,="" transforming="" growth="" factorβreceptor;α-sma,a-smooth="" muscle=""> |
Discussion
Le diabète est une maladie métabolique et le trouble du métabolisme du glucose en est la principale manifestation clinique. Au cours des dernières années, l'incidence de cette maladie n'a cessé d'augmenter(22). Le diabète entraîne des dommages et un dysfonctionnement de plusieurs organes. Les lésions rénales induites par le diabète sont l'une des principales causes de mortalité chez les patients diabétiques(23). Les principales manifestations cliniques dediabétiquenéphropathiese sont révélées être une protéinurie et un déclin persistant de la fonction rénale (24). De plus, l'apparition et le développement dediabétiquenéphropathieont été révélés favoriser le développement des maladies cardiovasculaires (25). Par conséquent, la nécessité de développer une nouvelle thérapie pour supprimer les dommages causés pardiabétiquenéphropathiechez les patients est urgent.
L'apeline est un facteur de graisse dans les tissus adipeux. Une étude récente a rapporté que l'apéline pourrait soulager les manifestations cliniques des patients diabétiques en régulant la glycémie (26). Une autre étude récente a rapporté que l'apéline-36 pouvait inhiber la sécrétion d'insuline induite par une concentration élevée de glucose (16,7 mmol/), mais n'avait aucun effet sur la sécrétion d'insuline induite par une faible concentration de glucose (2,8 mmol/)(27). Dans le corps des souris obèses et résistantes à l'insuline, l'apéline pourrait soulager la résistance à l'insuline et restaurer l'utilisation du glucose dans le corps (28). Cependant, dans le domaine dediabétiquenéphropathie, une étude récente a rapporté que les taux d'apéline et de son récepteur APJ dans le sérum de patients atteintsdiabétiquenéphropathieont été augmentés, et des niveaux plus élevés d'apeline et d'APJ ont favorisé la formation de vaisseaux sanguins et induit la prolifération des capillaires glomérulaires, favorisant ainsi l'apparition et le développement dediabétiquenéphropathie(29). Cependant, une étude différente a également indiqué queapelin-13pourrait inhiber la transformation des cellules épithéliales tubulaires rénales dans un environnement riche en glucose, inhibant ainsi l'apparition et le développement du processus EMT dans les cellules glomérulaires, retardant finalement l'apparition dediabétiquenéphropathie(30). Dans la présente étude, il a été démontré que l'utilisation deapelin-13diminué les niveaux de glucose dans le sang et soulagé la résistance à l'insuline chez ces rats. ainsi que réduit la teneur en protéines urinaires.Apéline-13le traitement a également atténué les dommages considérables induits par le glucose dans les cellules endothéliales des vaisseaux glomérulaires. Collectivement, ces résultats indiquent que l'utilisation deapelin-13soulagé les manifestations dediabétiquenéphropathie.
Une étude précédente a révélé que l'apéline pouvait réduire la teneur en glucose sanguin en régulant l'expression d'eNOS et en activant la voie Akt (31). L'expression de l'apéline pourrait également produire du NO en activant l'APJ, soulageant ainsi les manifestations cliniques dediabétiquenéphropathie(32).APJ est le récepteur deapelin-13, etapelin-13pourrait exercer ses effets biologiques en se liant à l'APJ (33). Dans la présente étude, la production de NO et l'expression d'eNOS et d'APJ ont également été détectées. Il a été révélé que les niveaux d'expression d'eNOS et d'APJ étaient augmentés dans les tissus rénaux et les cellules endothéliales des vaisseaux glomérulaires après un traitement avecapelin-13. La production de NO a également été augmentée dans les tissus rénaux des rats après un traitement avecapelin-13. Ces résultats ont indiqué queapelin-13favorisé l'expression d'eNOS en activant APJ. Par conséquent, des niveaux plus élevés d'eNOS ont amélioré la production de NO, favorisant finalement la perméabilité vasculaire et la filtration rénale.
Des études récentes ont indiqué que la fibrose rénale est une caractéristique dediabétiquenéphropathie(34,35). Les résultats de la présente étude ont révélé que l'expression de la E-cadhérine était améliorée dans les cellules et les tissus rénaux après un traitement avecapelin-13, tandis que celle de l'a-SMA a été diminuée.Apéline-13un traitement a également été révélé pour soulagerdiabétiquenéphropathieen supprimant la fibrose des tissus rénaux et des cellules endothéliales des vaisseaux glomérulaires.
En conclusion, la présente étude rapporte les effets deapelin-13sur le développement dediabétiquenéphropathie. Les résultats de la présente étude ont révélé queapelin-13atténuédiabétiquenéphropathieen favorisant la production de NO et en soulageant la fibrose dans les tissus rénaux. Cependant, la présente étude a aussi une limite. Le stress oxydatif et l'inflammation jouent un rôle important dans le développement dediabétiquenéphropathie(36-40). Qu'il s'agisseapelin-13améliorénéphropathie diabétiqueen réduisant l'inflammation et le stress oxydatif justifie une enquête dans notre future étude.

Références
1. Yu SY, Dong B, Fang ZF, Hu XQ, Tang L et Zhou SH : le renversement de l'ARNnc AK139328 atténue les lésions d'ischémie/reperfusion myocardique chez les souris diabétiques en modulant miR-204-3p et en inhibant l'autophagie. J Cell Mol Med 22 :4886-4898."2018.
2. Rowley WR et Bezold C : Créer une sensibilisation du public : Prévisions du diabète de l'État pour 2025. Popul Health Manag 15 : 194-200.2012,
3. Rowley WR. Bezold C.Arikan Y, Byrne E et Krohe S : Diabète 2030 : perspectives d'hier, d'aujourd'hui et des tendances futures. Gestion de la santé populaire 20 ; 6-12.2017.
4. American Diabetes Association : Standards of medical care in diabetes-2014.Diabetes Care 37(Suppl 1) : S5-S13.2014.
5. Ahlqvist E, van Zuydam NR, Groop LCand McCarthy MI : La génétique des complications diabétiques. Nat Rev Nephrol 11 :277-287. 2015.
6. Navarro-Gonzalez JF, Jarque A, Muros M, Mora C et Garcia J : Le facteur de nécrose tumorale alpha comme cible thérapeutique pourdiabétiquenéphropathie.Facteur de croissance des cytokines Rev 20 ; 165-173.2009.
7. Alvarez ML et Distefano JK : Le rôle des ARN non codants dansdiabétiquenéphropathie: Applications potentielles en tant que biomarqueurs pour le développement et la progression de la maladie. Diabetes Res Clin Pract 99 :1-11,2013.
8.Del Ry S, Cabiati M, Raucci S, Simioniuc A, Caselli C, Prescimone T et Giannessi D : séquençage et expression cardiaque d'Apelin dans Sus Scrofa. Pharmacol Res 60 : 314-319,2009.
9, Fasshauer M et Bluher M : Adipokines dans la santé et la maladie. Tendances Pharmacol Sci 36 : 461-470.2015.
10. Lv D, LiH et Chen L : Apelin et APJ, un facteur critique noel et une cible thérapeutique pour l'athérosclérose. Acta Biochim Biophys Sin(Shanghai) 45 527-533.2013.
11. Wysocka MB. Pietraszek-Gremplewicz K et Nowak D : Le rôle de l'apéline dans les maladies cardiovasculaires, l'obésité et le cancer. Avant Physiol 9 : 557.2018.
12.Sentinelli F, Capoccia D., Bertoccini L,Barchetta I,Incani M, Coccia F, Manconi E,Lenzi A,Cossu E.Leonetti F, et al :Recherche d'une variante génétique dans le gène de l'apeline par reséquençage et association étude sur des sujets européens, Genet Test Mol Biomarkers 20 ;98 102,2016.
13. Onalan E, Yakar B, Barim AO et Gursu MF : taux sériques d'apéline et de résistine chez les patients présentant une altération de la glycémie à jeun, une altération de la tolérance au glucose, un diabète de type 2 et un syndrome métabolique. Endokrynol Pol 71 :319-324, 2020.
14. Adki KM et Kulkarni YA : biomarqueurs potentiels dans la rétinopathie diabétique. Curr Diabète Rév 16 : 971-983.2020.
15. Wu R, Zhu Zand Zhou D : VEGF, apéline et HO-1 chez les patients diabétiques atteints de rétinopathie : une analyse de corrélation. BMC Ophthalmol 20 : 326.2020.
Noter:ce qui précède n'est pas une liste de référence complète
